Laborvezető: Krenács Tibor, PhD, DSc
A laboratórium elsősorban daganat-progressziós, -prognosztikai és -predikciós biomarkerek kutatásával és validálásával, valamint a modulált rádiófrekvenciás (13,56 MHz) elektromos tér daganatkárosító hatásának tanulmányozásával foglakozik. Munkát in situ molekuláris morfológiai módszerek (imunhisztokémia, in situ hibridizáció), nagyléptékű szöveti „microarray” (TMA), digitális mikroszkópia és automatizált mennyiségi képanalízis támogatják. Megfigyeléseket szükség esetén in vitro molekuláris, fehérje expressziós, valamint sejttenyészetben és állatmodelleken végzett funkcionális vizsgálatok egészítik ki.
Főbb projektek:
1) Modulált elektrohipertermia (mEHT) daganatellenes hatásának hatásmechanizmusa és a kombinált mEHT + célzott terápiás kezelések optimalizálása
Háttér: A malignus daganatok fokozott glükolízise (Warburg hatás) és ionkoncentrációja miatt bennük a az elektrohipertemiával közvetített elektromos tér és a következményes hő (<42oC) feldúsul, ami hozzájárul szelektív károsításukhoz.
Modell, vizsgálati anyag:
– in vivo: – colorectális carcinoma sejtvonal xenograftok (HT29) ill. allograftok (C26) egérben
– emlőcarcinoma sejtvonalak (tripla negatív, ill. HER2 pozitív) egér allograftok kombinált
mEHT+ immun„checkpoint”-ihibitor (Ipilimumab, Nivolumab) ill. Herceptin kezelése
– in vitro: -egér, ill. emberi eredetű konfluens daganat sejtvonalak (colorectális, emlő, ill. tüdő)
Vizsgáljuk:
– a programozott sejthatál sejttípus-függő mechanizmusát és az aktivált jelutakat
– a károsodás asszociált molekuláris mintázatot (DAMP) és immunogén faktorokat
– indukált tumorellenes sejtes immunválaszt
– a szisztémás, távol-(„abscopal”) hatást, kombinált kezelésekkel
– a daganatsejtek glükóz metabolizmusának és a kezelés hatékonyságának összefüggéseit
– a kezelés tumorszelektivitását
Fontosabb eredmények:
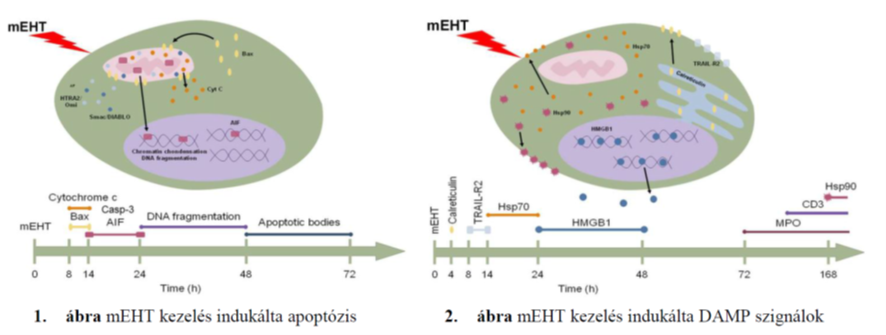
Állatokba ültetett daganat xeno-, illetve alograft modelleken igazoltuk, hogy az mEHT kezelés hatása a daganattípus genetikai és epigenetikai tulajdonságai alapján kaszpáz-függő, vagy független (apoptózis indukáló faktor -IAF vezérelt) programozott sejthalál úton valósulhat meg (1 . ábra), a stresszfüggő DAMP fehérjék (calreticulin, HSP70 és HMGB1) transzlokációja, majd felszabadulása (2. ábra) és a tumorellenes immunitás sejtjeinek (CD8+ citotoxikus sejtek és S100+ antigén-prezentáló sejtek) fokozott daganatinváziója kíséretében.
Releváns közlemények:
1. Andocs G, Meggyeshazi N, Balogh L, Spisak S, Maros ME, Balla P, Kiszner G, Teleki I, Kovago C, Krenacs T. Upregulation of heat shock proteins and the promotion of damage-associated molecular pattern signals in a colorectal cancer model by modulated electrohyperthermia. Cell Stress Chaperones. 2015, 20:37-46.
2. Meggyeshazi N, Andocs G, Balogh L, Balla P, Kiszner G, Teleki I, Jeney A, Krenacs T. DNA fragmentation and caspase-independent programmed cell death by modulated electrohyperthermia. Strahlenther Onkol. 2014, 190:815-822.
A munkacsoport tagjai:
Dr. Krenács Tibor, tudományos főmunkatárs
Mátrainé Balogh Éva, immunhiztokémiai szakasszisztens
Vancsik Tamás, PhD hallgató
Dr. Maros Máté Előd, külsős PhD hallgató
Dr. Forika Gertrud, önkéntes segítő (PhD pályázó)
Kiss Éva, biológus, önkéntes segítő
Egyéb aktivitás:
A Labor végzi a QualiCont nemzeti patológiai (technológiai) külső minőségbiztosítási program szakmai irányítását és részt vesz a HER2 célzott terápia diagnosztikájának hazai standardizálásában is.
További projektek:
2) Daganat-progressziós, -prognosztikai és -predikciós biomarkerek kutatása
A) Sejtciklusszabályozás in situ vizsgálata daganatokban
Háttér: Mind a növekedési jelutak, mind a sejtciklus szabályozás genetikai és/vagy epigenetikai deregulációja a malignus daganatok autonóm replikációjához vezet. A fokozott sejtciklus progresszió a daganatok agresszivitását jelzi és összefügg a kedvezőtlen prognózissal, valamint a kemoterápia hatékonyságát is előre jelezheti.
Modell, vizsgálati anyag:
– humán melanocytás daganatok: naevus, dysplasztikus naevus, vékony melanoma, vastag melanoma,
melanoma áttét
– humán tenyésztett melanoma (A2058, WM35, HT168, ill. HT199) és melanocyta sejtvonalak
– klinikailag követett együttműködésből származó (EuroBonet, EU FP6) primer és rekurrens óriássejtes
csonttumor (GCTB) szövetminták, valamint primer, tenyésztett neoplasztikus strómasejtek
– klinikailag követett osteosarcoma szövetminták, kezelési adatokkal
– együttműködések keretében emlőcarcinoma, ill. fej-nyaki carcinomák
Vizsgáljuk:
A tumor sejtciklus frakciók változásának kapcsolatát a
– daganatprogresszióval, ill.
– a prognózissal (betegségmentes, ill. teljes túlélés)
Fontosabb eredmények:
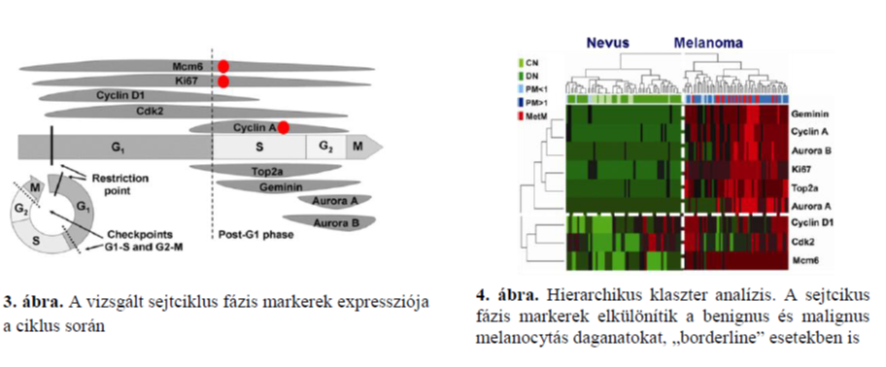
A naevusokban (dysplasticus naevusokban is) a sejtciklusba lépett daganatsejtek megrekednek a G1-fázisban. Az általános (Mcm6 és Ki67) sejtciklus marker pozitív sejtfrakciók szignifikáns emelkedése és a poszt-G1 fázis (Cyclin A+) sejtek megjelenése elkülöníti a primer vékony melanomákat a dysplasticus naevusoktól. Vastag melanomákban a sejtciklus progresszió szignifikánsan felgyorsult/fokozott a vékony melanomákhoz képest. Az áttétképzésre halamosító proliferatív fenotípus már vastag melanomákban kialakul. A Ki-67, MCM2, cyclin A, and PHH3 expresszió emlőcarcinomákban a primer szisztémás terápia patológiai komplett remisszióának előrejelzője. A GCTB progresszió és a sejtciklus szabályozás kapcsolatát vizsgáló munkánk közlés alatt van, míg az osteosarcoma hasonló alapú tanulmányozása folyamatban.
Releváns közlemények:
1) Kiszner G, Wichmann B, Nemeth IB, Varga E, Meggyeshazi N, Teleki I, Balla P, Maros ME, Penksza K, Krenacs T. Cell cycle analysis can differentiate thin melanomas from dysplastic nevi and reveals accelerated replication in thick melanomas. Virchows Arch. 2014, 464:603-612.
2) Tőkés T, Tőkés AM, Szentmártoni G, Kiszner G, Madaras L, Kulka J, Krenács T, Dank M. Expression of cell cycle markers is predictive of the response to primary systemic therapy of locally advanced breast cancer. Virchows Arch. 2016, 468:675-686.
2/B) Kollagén XVII (COL17A1) expresszió malignus daganatokban
Háttér: A kollagén XVII egy hemidezmoszolális fehérje, mely a differenciálatlan keratinocytákat a bazális membránhoz horgonyozza. Normálisan expressziója a kiérő keratinocytákban megszűnik. Tumorképződés során ez a negatív „feedback” mechanizmus károsodik, így a fehérje neo-expressziója az epidermális hám korai malignus transzformációját jelzi. A fehérje expresszióját melanomákban elsőként figyeltük meg.
Modell, vizsgálati anyag:
– humán melanocytás daganatok: naevus, dysplasztikus naevus, vékony melanoma, vastag
melanoma, melanoma áttét
– humán tenyésztett melanoma sejtvonalak (A2058, WM35, WM983B, HT168, HT199, ME24met, ill.
HT168M1)
– klinikailag követett emlőcarcinomák, együttműködésben (University of Qeensland, Australia)
Vizsgáljuk:
– a kollagén XVII expresszió (ekto- ill. endodomén specifikus antitestekkel) és a daganatprogresszió
viszonyát melanocytás daganatokban
– melanoma sejtvonalakban a fehérje és mRNS szinteket párhuzamosan
– a melanoma sejtvonalak specifikus antitest kezelésének hatását
– a fehérje kifejeződését egérben növesztett primer és áttéti melanoma (HT199) xenograftokban
– a fehérje expresszió és a gén promoter metilációjának kapcsolatát emlőcarcinoma progreszió során
Fontosabb eredmények:
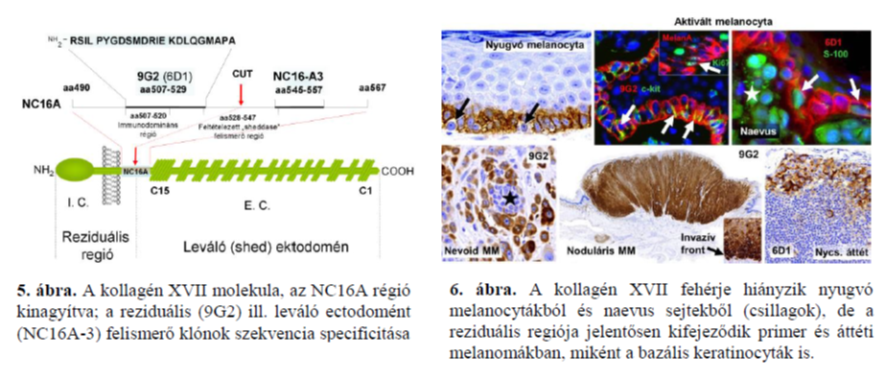
A kollagén XVII fehérje 60kDa-os reziduális doménje (5. ábra) nyugvó melanocytákban nem mutatható ki, míg a fehérje kifejeződése melanocytás daganatokban a malignus transzformáció és a daganat invazivitás markerének bizonyult (6. ábra). A reziduális endodomén NC16A-os extracelluláris szakaszán keresztül a melanoma sejtek növekedése doménspecifikus antitest (9G2 klón) kezeléssel célzottan gátolható. Míg bőr, vagy cervix laphámcarcinomákban a kollagén XVII fehérje expressziója felülregulát, emlőcarcinomákban a gén promoter metilációja miatt ez szignifikánsan csökkent, amit utóbbi daganatoknál fokozott invazivitás is kisér.
Releváns közlemények:
1) Thangavelu PU, Krenacs T, Dray E, Duijf PH. In epithelial cancers, aberrant COL17A1 promoter methylation predicts its misexpression and increased invasion. Clin Epigenetics. 2016 Nov 18;8:120.
2) Krenacs T, Kiszner G, Stelkovics E, Balla P, Teleki I, Nemeth I, Varga E, Korom I, Barbai T, Plotar V, Timar J, Raso E. Collagen XVII is expressed in malignant but not in benign melanocytic tumors and it can mediate antibody induced melanoma apoptosis. Histochem Cell Biol. 2012, 138:653-667.
3) Stelkovics E, Korom I, Marczinovits I, Molnar J, Rasky K, Raso E, Ficsor L, Molnar B, Kopper L, Krenacs T. Collagen XVII/BP180 protein expression in squamous cell carcinoma of the skin detected with novel monoclonal antibodies in archived tissues using tissue microarrays and digital microscopy. Appl Immunohistochem Mol Morphol. 2008, 16:433-441.
2/C Connexin expresszió és csatornafunkciók szerepe daganatok progressziójában
Háttér: A connexin tertaspan molekulák hexamerekké oligomerizálódva az extracelluláris tér kizárásával direkt sejt-sejt kommunikációs csatornákat képeznek a szomszédos sejtek membránjában. A csatornákon <1,8 kDa ionok, metabolitok, morfogének és másodlagos hírvivők szabályozottan közlekednek az összekapcsolt sejtek között. A csatornák fontos szerepet játszanak a morfogenezisben, szövet-regenerációban és az adaptív sejtválaszok összehangolásában. Daganatprogresszió során a connexinek expressziója csökken, de re-expressziót is megfigyeltek tumorinvázió és metasztázisképzés kapcsán.
Modell, vizsgálati anyag:
– klinikailag követett, együttműködésből származó (EuroBonet, EU FP6) primer és rekurrens óriássejtes
csonttumor (GCTB) szövetminták, valamint primer, tenyésztett neoplasztikus strómasejtek
– reaktív tonzillából izolált, majd tenyésztett alacsony denzitásaú sejtfrakció (ex vivo follikulusok), ill.
follikuláris lymphomák
– in silico, connexin izotípus mRNS expressziós adatbázisok (Affimetrix, ill. Illumina) elemzése
emlőcarcinomákban
– klinikailag követett, hazai (SE, II-es Patológia) és nemzetközi (Zürich-i Egyetem) együttműködésből
származó elmőcarcinomák
Vizsgáljuk:
– a connexin43 (Cx43) expresszió és csatornafunkciók kapcsolatát a GCTB daganat progressziójával
– a connexin expresszió és csatornagátlás (Gap27 Cx mimetikus peptiddel) szerepét ex vivo
csíracentrumok kialakulásában, ill. follikuláris lymphomák (FL) progressziójában
– a connexin izotípusok expressziója és az emlőcarcinomák progressziója, valamint prognózisa közötti
összefüggéseket
– primer szisztémás kemoterápiával kezelt emlőcarcinomák connexin expressziójának és a kezelés
hatékonyságának összefüggéseit
Fontosabb eredmények:
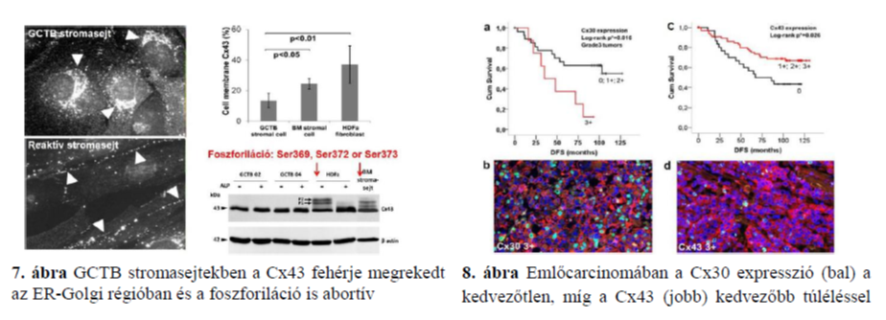
A Cx43 kommunikációs csatornák deregulációja (7. ábra) GCTB neoplasztikus stromasejtekben a csökkent osteoclastogenikus kontroll miatt hozzájárul a GCTB klinikai progressziójához és a rosszabb prognózishoz. A Cx43 csatornák gátlása az ex vivo csíracentrumok abortív fejlődését eredményezi, jelentős follikuláris debndritikus sejt és B-sejt pusztulással, de a Cx43 expresszió nem mutat szignifikáns kapcsolatot az FL progresssziójával. Emlőcarcinomákban a connexin izotípusok típus/stádiumtól függő szelektív expressziót mutatnak, akár tumorszupresszor (pl. Cx43, Cx46), akár tumor promoter (Cx30) szerepük lehet (8. ábra), így meghatározásuk független pozitív, ill. negatív prognosztikus markerként szolgálhat.
Releváns közlemények:
1. Balla P, Maros ME, Barna G, Antal I, Papp G, Sapi Z, Athanasou NA, Benassi MS, Picci P, Krenacs T. Prognostic impact of reduced connexin43 expression and gap junction coupling of neoplastic stromal cells in giant cell tumor of bone. PLoS One. 2015 May 1;10(5):e0125316.
2. Rajnai H, Teleki I, Kiszner G, Meggyesházi N, Balla P, Vancsik T, Muzes G, Csomor J, Matolcsy A, Krenacs T. Connexin 43 communication channels in follicular dendritic cell development and in follicular lymphomas. J Immunol Res. 2015;2015:528098.
3. Teleki I, Szasz AM, Maros ME, Gyorffy B, Kulka J, Meggyeshazi N, Kiszner G, Balla P, Samu A, Krenacs T. Correlations of differentially expressed gap junction connexins Cx26, Cx30, Cx32, Cx43 and Cx46 with breast cancer progression and prognosis. PLoS One. 2014 Nov 10;9(11):e112541.
4. Teleki I, Krenacs T, Szasz MA, Kulka J, Wichmann B, Leo C, Papassotiropoulos B, Riemenschnitter C, Moch H, Varga Z. The potential prognostic value of connexin 26 and 46 expression in neoadjuvant-treated breast cancer. BMC Cancer. 2013 Feb 2;13:50.