Bevezetés
A nyaki verőérszűkület terápiája a stroke-ok egy részében jelenthet megelőző kezelést.
A téma kiemelt jelentőségét az adja, hogy a világon és így Európában is a stroke a második leggyakoribb halálok.
Magyarországon több, mint 21.000 stroke fordul elő évente, és 14.000-t meghaladja a szélütéshez köthető halálozás. A heveny agyi katasztrófák patomechanizmusa alapján az esetek kb 85%-át ischaemiás kórképek adják és csak körülbelül 15%-ban vérzéses kóreredet van a szöveti károsodás hátterében. Az ischemiás stroke-ok pontos meghatározása az esetek közel negyedében nem sikerül. Az összes ischemiás stroke közel 15-30%-ért felelős az agyi vérellátásban szerepet játszó erek szűkülete, ennek 60-70% az extracranialis carotis szűkület.
1.0 Stroke
A World Health Organization (WHO) által 1980-ban megfogalmazott definíció szerint a stroke:
Gyorsan kialakuló, fokális vagy esetenként globális, 24 óránál hosszabb ideig tartó (vagy halált okozó) neurológiai funkciókieséssel járó tünet együttes, melynél vaszkuláris eredeten kívül más ok nem merült fel. A globális tünetek ebben a megfogalmazásban csak a subarachnoidális vérzést elszenvedő betegekre értendő. A tranziens ischaemiás attack (TIA) azonos jellegű elváltozás, amelynek időtartama <24h. A mai napig is a klinikumban, kutatásban és számos vezérfonalban ez a definíció szerepel. A modern képalkotókkal végzett vizsgálatok azonban egyértelműen mutatják, hogy a tünetek időtartama és a kimutatható definitív ischaemiás elváltozások nem köthetők össze a korábbi 24 órás kritériummal. A 2013-ban megjelent American Heart Association/American Stroke Association (AHA/ASA) vezérfonalban megpróbálták a definíciót ennek megfelelően átalakítani: Agyi, gerincvelői vagy retinális sejtek ischaemia vagy vérzés miatti pusztulását jelenti, amelyet neuropatológiai, képalkotó vagy más objektív módon bizonyítani lehet illetve, olyan klinikailag bizonyítható agyi, gerincvelői vagy retinális fokális, ischaemiás károsodás, amelynél a tünetek időtartama> 24 óra, vagy a beteg halálakor is észlelhetőek valamint más okok a tünetek mögött kizárhatóak. A TIA kifejezés helyett az AHA/ASA ajánlás a tünetek időtartamának és a definitív, valamely módon kialakult végleges szövetpusztulást javasolja figyelembe venni. Az AHA/ASA által megfogalmazott definíció arra hívja fel a figyelmet, hogy nem a tünetek időtartama, hanem bekövetkező permanens sejthalál a stroke jellemzője.
1.1.1 Stroke etiológia
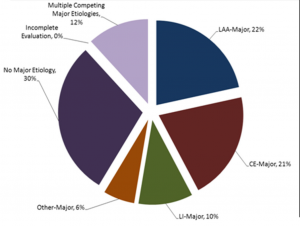
Az ischemiás stroke kiváltó okaként már évtizedek óta használt beosztás (TOAST) megkülönböztet: 1, nagy artériákat érintő atheroszklerózist; 2, kardioembolizációt; 3, kis ereket elzáródását; 4, stroke egyéb okok miatt, valamint 5, nem meghatározható okot. A kis erek elzáródását lacunaris infarktusnak is szokták nevezni. Az egyéb okok között is előfordul a közepes és nagyobb ereket érintő patológia, például a disszekció, Moya-moya, fibromuszkuláris diszplázia, vaszkulitis, koagulopátia. A nagyobb erek által okozott stroke-ot korábban 30% körülinek gondolták, jelenleg inkább a lacunaris, kis erek elzáródásából eredő szélütések számát tartják többnek, és a nem meghatározható okok között feltehetően sokszor van fel nem ismert szívritmus-zavar. Összességében az előbbiek alapján az ischemiás stroke-ok közel 20%-át tartják carotis eredetűnek.
1.1. 2 Stroke incidencia változása
Több vizsgálat is feltételezi, hogy a stroke előfordulása az utóbbi évtizedekben csökkent. Azonban van olyan tanulmány, amely az incidenciát stabilnak véli. Több európai ország és az USA adatait felhasználva Zhang és munkatársai nem tudták igazolni az incidencia csökkenését. A növekedés mellett szólna a növekvő életkor és a diabetes előfordulásának aránya.
1.2 A carotis szűkület és a stroke összefüggése
Az ischaemiás szélütések közel 10-20%-ért felelős a nyaki verőér szűkülete. A carotis oszlásban elhelyezkedő atheroszklerotikus plakk szerkezete megegyezik más érszakaszban található elváltozásokkal. Bár a stroke-ot okozó pontos mechanizmus nem ismert, de feltételezhetően az esetek nagy részében nem a szűkület okozta haemodinamikai okok, hanem az atheroszklerotikus plakk kapcsán létrejövő thrombo-embolizáció a felelős a szélütések kialakulásáért. A legelfogadottabb nézet szerint a plakkban lévő koleszterin kristályok szerepet játszanak az embolizációban
2., A carotis szűkület előfordulása, kialakulásának rizikófaktorai
Egy norvég vizsgálatban (Tromso study) 35%-os vagy annál nagyobb lumen csökkenést számolva, a carotis szűkület prevalenciája (előfordulása) 3,8% volt a férfiaknál és valamivel kevesebb 2,7% volt a nőknél.
Egyéb rizikók:
• életkor (50év felett folyamatosan emelkedik)
• dohányzás
• ismert érszűkület a kórtörténetében
• koronária-betegség
• korábban stroke előfordult
Mindkét carotis interna együttes szűkületének előfordulása magas, közel 30%.
2.1 A carotis szűkület specifikus etiológiája, a szűkület lokalizációja
Az atheroscleroticus plakk kialakulásának leggyakoribb helye a carotis interna-externa oszlásban található kiszélesedő carotis bulbus. Amelynek oka feltehetően a turbulens áramlás, pontosabban a lamináris áramlás alatt normálisan magas nyíróerő hiánya, amely több mediátoron keresztül gátolja az endotheliális sejtek proliferációját.
3.0 Diagnosztika
Auscultatio
Önmagában diagnózis felállítására nem alkalmas, szűrő jellegű vizsgálat. A carotis feletti zörej nem jelzi megbízhatóan a 60-70% feletti szűkület meglétét. Nincs a carotis szűkületek diagnosztikájában szerepe. Szűrő jelleggel csak a kiemelt rizikócsoportban van értelme végezni.
Ultrahang
A duplex ultrahang a carotis diagnosztikában az elsőként választandó módszer, mivel olcsó, non-invazív és jó vizsgáló esetében rendkívül pontos. Az ultrahanggal az áramlási sebességek alapján lehet következtetni a szűkület nagyságára, a szűkületben mért körülbelül 230 cm/s-os áramlási sebesség felel meg a NACET szerinti 70%-os szűkületnek, a 90%-os stenosis közel 400 cm/s-os sebességet jelent.
A carotis duplex ultrahang az egyik legpontosabb vizsgáló módszer, főleg a 70%-nál nagyobb szűkület megállapítására.

CTA
Az UH vizsgálatnál objektívebb, elérhetőségük rosszabb, de hazánkban szinte mindenhol hozzáférhető. Előnyt jelent, hogy a koponya ischaemiás lézióiról és az aorta ívtől az intracranialis erekig értékelhető képet ad, amely esetleges rekonstrukció esetén annak tervezésében jelentős segítség. Hátránya, hogy kontrasztanyag adása szükséges, és az ionizáló sugárzás.
MRA
Jelenleg a multidetectoros CTA (MDCTA) adja a legpontosabb képet egy esetleges műtét vagy intervenció előtt. Csak speciális indikációk esetén javasolt MRA – pl. kontrasztanyag-allergia

3.2 Carotis szűkület meghatározása képalkotókkal
Szűkület mértéke CTA, MRA, DSA alapján
Az ACI/ACC szűkület meghatározására két elfogadott módszer létezik (Ábra):
• NASCET (North American Symptomatic Carotid Endarterectomy Trial) a legkisebb reziduális átmérőt a disztális, ép ACI szakasszal hasonlítjuk össze
• ECST – European Carotid Surgery Trial a legkisebb átmérőt ugyanebben a szintben az eredeti átmérővel hasonlítjuk össze
A két mérési módszer közül a NASCET az elterjedtebb.A két mérési módszer közül az ECST ad meg nagyobb értékeket általában. Ábra, NASCET – ECST szűkület
4. Terápia
A szignifikáns carotis stenosis terápiájának célja a stroke prevenció. Primer az aszimptomatikus betegeknél illetve secunder a tünetes betegcsoportban.
Carotis szűkület esetén talán logikusabb a terápiás lehetőségeket előbb megbeszélni, mint a pontos indikációs folyamatot, mivel az nem is áll másból, mint a beavatkozás nélküli stroke ráta összehasonlítása a másik két terápiás lehetőség posztoperatív rizikóival. Alapvetően három lehetőség közül választhatunk, nyitott műtét, endovaszkuláris kezelés, vagy gyógyszeres kezelés.
4.1 Nyitott műtét
Alapvetően három módszer jön számításba, a hagyományos endarterectomia, az eversios endarterectomia és az interpositum beültetése. A műtétek döntő többsége valamelyik endarterectomia, amely az érfal belső – meszes- rétegének eltávolítását jelenti.
4.1.2. Endarterectomia
Az a. carotis extracranialis szakaszának kezdeti része, ahol az érszűkület jellemzően elhelyezkedik, nyitott műtéttel könnyen elérhető. A feltárásnak, annak ellenére, hogy fontos képletek futnak a közelében, szerencsére ritkán vannak tartós, jelentős életminőséget rontó szövődményei. A lézió általában rövid 1 -2 cm hosszú, így a lehetséges rekonstrukciók közül az endarterectomia adja a legjobb eredményeket.
4.1.2.1 Hagyományos endarterectomia
A műtét történhet a m. sternocleidomastoideus mentén vezetett metszésből és haránt nyaki metszésből is. A műtét során az ACC disztális szakasza, valamint az ACE és ACI kerül feltárásra – általában a v. jugularistól medialisan a v. facialis lekötése után. Heparinizációt követően kirekesztés (általában érdemes az ACI-vel kezdeni, az embolizáció lehetőségének csökkentésére), majd egy hosszanti tomia az ACC ép szakaszáról az ACI ép szakaszára. Ekkor van lehetőség a shunt behelyezésére. Nyitott endareterctomia után a disztális (az ACI-n), illetve szükség esetén a proximális (ACC) intima-lépcsőt le lehet ölteni. A tomia zárására a magasabb restenosis arány miatt nem javasolják a rutin direkt érvarrat alkalmazását, műér darabbal vagy xenografttal (bovin) történhet az ér rekonstrukciója. (Ábra) A bovin pericardiumból készült folttal alacsonyabb volt a posztoperatív vérzések száma, és az első évben észlelt resztenózisok aránya. A perioperatív stroke és TIA arányában a bovin és Dacron folt hasonlóan megelőzte a primer zárás, vénás vagy PTFE folt eredményeit.
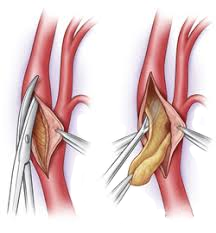

4.1.2.2. Everziós endarterectomia
Az ACI eredését átvágjuk az ACC oszlásnál, a rétegképzés után az érfal külső részének visszafordításával történik az endarterectomia. A műtét kritikus pontja az endarterectomia disztális zónája, ahol a megvastagodott szakasz átmegy az ép részbe, mivel nincs lehetőség az intima-lépcső leszegésére. Az ACI eredésnek helyről az ACC-ACE nyitott endarterectomiáját végezzük. Végül a „kitisztított” proximális ACI szakaszt visszafordítva rekonstruáljuk a bulbust.

4.1.2.3 Az everziós és hagyományos endarterectomia összehasonlítása:
A hagyományos és everziós technika között nincsenek jelentős különbségek a mortalitás, postoperatív stroke arányában, amennyiben a hagyományos technika során a tomia zárása folttal történik. Az eveziós endarterectomiához nem szükséges foltplasztika, nincs idegen anyag (így kevesebb az infekció, késői folt-degeneráció), kevesebb az embolizáció, kevesebb a késői restenosis, hosszabb, elongált ACI rekonstrukciója könnyebb, a műtéti idő rövidebb. Hátránya: shunt használata nehézkesebb, mert a shunt behelyezése előtt az endarterectomiát legalább részben el kell végezni. A disztális intima-lépcső ellátása esetenként nehéz lehet, illetve gyakoribb a posztoperatív magasvérnyomás.
4.1.3. Áthidalás (interpositum)
Általában a szokásos léziótól eltérő esetekben használt módszer, amikor az atheroszklerotikus plakk nagyon hosszú, a környezet erősen heges, gyulladásos vagy tumor miatt nem marad vissza olyan érfal, amely az endarterectomiát lehetővé teszi.
4.1.4 Carotis kirekesztés alatti stratégiák
Alapvetően három startégia lehetséges. Vannak, akik állandóan shunt védelemben végzik a műtéteket, vannak szelektív shunt használók, és vannak, akik soha nem használnak shunt-öt. A műtéti típus választása alapvetően befolyásolja a stratégiát, mivel eversios endarterectomia során nehézkesebb a shunt használata. A kifordított ACI-be kell a shunt-öt behelyezni, és azt is csak akkor lehet, amikor az ér már az endarterectomia érdemi része kész. Aki everziós technikát használ, általában nem szeret shun-öt használni, illetve fordítva is igaz, aki valamiért shunt használata mellett dönt, inkább a hagyományos, hosszanti tomiát választja.
Egyik módszer sem jobb a többinél. Az állandó shunt használat során sok betegnél felesleges manipulációt jelent, amely esetleges dissectioval járhat, a mikroembolizáció veszélye áll fent. Elvileg a szelektív shunt használata lenne a legjobb, azonban ezzel a stratégiával előfordulhat akár kiemelkedően rossz postoperatív stroke ráta is, ha a próba-kirekesztés és a shunt behelyezésének stratégiája, technikája nem megfelelő. Sokan úgy vélik, hogy bizonyos neuromonitor-módszerek során csak későn észlelik az ischemiát. Az állandó shunt nélküli stratégia pedig nyilvánvalóén hordozza magában az esetleges áramlási hiányból eredő neurológiai szövődményeket.
4.1.4.1 Szeletív shunt használata – neuromonitorizálás
Jelenleg többféle neuromonitorizálás létezik, EEG, transzkraniálisan kiváltott vagy detektált motoros és szenzoros potenciál monitorizálása, agyi oxigén- szaturáció mérése infravörös közeli fénnyel, kirekesztés után az ACI-ben mért nyomás, valamint transzkraniális dopplerrel az a. cerebri media áramlásának mérése. Jelenleg egyedül a loco-regionális anaesthesiában végzett műtéteket fogadják el, mint effektív neuromonitorizálás. Ilyenkor a beteg kontaktusba vonható, neurológiai statusa könnyen monitorizálható. Azonban az altatásban végzett műtétekhez képest perioperatív stroke aránya nem jobb.40 Történnek preoperatív vizsgálatok is annak meghatározására, hogy melyik betegnél várható, hogy kirekesztés alatt nem lesz megfelelő az agyi vérellátás, bár vannak bíztató eredmények evidencia szintű megállapítástól még messze vagyunk.
4.1.5.Lehetséges műtéti szövődmények:
- perioperatív stroke (embolizáció, áramlási hiány)
- perioperatív myocardialis infarktus
- cerebralis hiperperfúziós szindróma
- perifériás idegkárosodás (n. laryngeus recurrens, n. hypoglossus. n. facialis) -egyik leggyakoribb a nyaki bőrideg sérülése miatti érzéskiesés a fül környékén
- vérzés, haematoma
- restenosis
4.2 Endovaszkuláris
A minimál-invazív endovaszkuláris terápia megjelenésével természetesen megkezdődött a carotis szűkület endovaszuláris kezelése is. Logikusnak tűnt, hogy potenciális alternatívája lesz a carotis endarterctomiának. Az első próbálkozások az 1970-es évek végén kezdődtek. Eleinte csak ballonos tágítást végeztek stent beültetés nélkül, majd az 1980-as végén ballonra rögzített stentekkel próbálkoztak, eleinte meglehetősen rossz eredménnyel. Ez a helyzet az öntáguló stentek, és az embóliás szövődmények csökkentését szolgáló eszközök megjelenésével jelentősen javult. Szélesebb használatát talán a SAPPHIRE vizsgálat sikere után számíthatjuk, ahol magas sebészeti rizikóval rendelkező betegcsoporton hasonlították össze az endarterectomia eredményeivel. Bár számos multicentrikus vizsgálat az endarterectomiánál jelentősen rosszabb neurológiai szövődmény-rátát talált, azért az is nyilvánvalóvá vált, főleg az előbb említett SAPPHIRE és CREST vizsgálatok alapján, hogy megfelelő operatőr és helyes betegkiválasztás esetén – főleg a tünetmentes betegcsoportban – jelenthet alternatívát a nyitott műtéttel szemben.
Ábra – stent és stent impl.
A terápia lényege a carotis bulbusban lévő plakk deformálása és lefedése, amelynek következtében a plakkból eredő embolizáció csökken. A legjobb eredményeket a zárt cellás szerkezetű sztentek adták, ahol az érfalban lévő plakk nehezebben tud a lumen felé kiboltosulni az implantáció után. A beavatkozást femoralis, brachiális és radiális szúrásból is biztonságosan el lehet végezni. A disztális embóliavédelem hatásosságára jelenleg nincs evidencia, annak ellenére, hogy gyakran találnak plakk törmelékeket a beavatkozások során használt disztális filterben.
Az intervenciót végző centrum rutinja a carotis endarterectomiához hasonlóan fontos. Általában minimum 2 éves gyakorlat szükséges ahhoz, hogy a perioperatív stroke ráta 5% alá csökkenjen. Egyes szakértői vélemények szerint közel 25 beavatkozás szükséges a kompetencia megszerzéséhez és évente legalább 10 beavatkozás annak fenntartásához.
Az idősebb betegcsoportban rosszabbak a sztentelés eredményei, mint a fiataloknál, feltehetően az aortaív kiterjedtebb meszesedése miatt, amelyből az embolizáció gyakoribb lehet. A kezelni kívánt lézió hossza ugyancsak független rizikófaktor több tanulmány szerint is.
4.3 Konzervatív kezelés (optimal (vagy) best medical therpy – BMT)
4.3.1. Thrombocyta aggregáció gátlás
A thrombocyta aggregáció gátlás köztudomásúan csökkenti a stroke kockázatát, azonban gasztrointesztinális vérzés rizikóját is emeli.
Acetil-szalicilsav v. clopidogrel monoterápia javasolt
Az újabb hatóanyagok:
• Ticagrelor kapcsán nem írtak le eddig jobb eredményeket.
• Prasugrelről csak koronária megbetegedés kapcsán van adat, TIA/stroke után jelenleg kontraindikált az adása
• Cangrelor pedig jelenleg nincs oralis gyógyszer formájában forgalmazva.
4.3.2. Statin
Számos randomizált vizsgálat írja le a statin kezelés hatásosságát a koronária megbetegedés kapcsán csupán minimális mellékhatások mellett.
4.3.1. Rizikófaktorok csökkentése
Egyszerű lenne leírni, hogy beavatkozás nélküli kezelés valamilyen thrombocyta aggregáció-gátló és statin szedését jelenti, azonban ez így nem teljesen igaz.
Az optimális kezelés alapja a bizonyítottan jelentős rizikófaktorok csökkentése:
• dohányzás
• fizikai inaktivitás
• elhízás
• nem kezelt magas vérnyomás
• egészségtelen táplálkozás
Feltehetően a rendszeres nyaki ultrahang kontroll helyett sokkal több szélütést lehetne megelőzni, ha sikerülne valami módon elérni a betegeknél rizikófaktoraik csökkentését. A közepes és magas fizikai aktivitás más rizikófaktorok csökkentésével (magas vérnyomás, testsúly) 25%-os relatív ischemiás stroke rizikó csökkentését jelenti
Terápiás döntés folyamata
5.1 Tünetmentes (symptomaticus) carotis szűkület
Jelentős különbség van a tünetes és tünetmentes carotis stenosis között egy újabb stroke előfordulásának veszélye tekintetében.
Tünetmentes betegeknél az éves stroke ráta a konzervatív kezelés mellett csupán 0.7-2.2%/év. Ennek alapján elmerül a kérdés, ha ilyen alacsony a stroke arány, miért kell egyáltalán tünetmentes betegeket operálni? A jelentős bénulással járó stroke-ok nagy részében azonban nincsen korábbi illetve bevezető tünet. Az a carotis endarterectomián átesett betegeknél (6%) feleannyi stroke volt 5 év alatt (a 3%-os perioperatív stroke arányt is beleszámítva), mint a konzervatív terápián lévőknél 12%.
Jelenleg érvényben lévő magyar ajánlás szerint 70% feletti carotis szűkületnél lehet műtét mellett dönteni, amennyiben a várható élettartam eléri az 5 évet, és olyan centrumokban kell a beavatkozásokat elvégezni, ahol a perioperatív stroke ráta alacsony.
5.1.1. Nemek közti különbségek:
A konzervatív terápia mellett kevesebb stroke volt nőknél évente, így több idő kellett ahhoz, hogy a műtét preventív hatása szignifikánssá váljon, ezért nőknél inkább a 10 év várható élettartamot kell figyelembe venni.
5.1.2 Szűkület mértékének növekedése
Gyógyszeres kezelés mellett is várható a tünetmentes betegeknél a szűkület mértékének növekedése. A tünetmentes betegek 45%-nak növekedett a nyaki érszűkülete.
5.1.3. Tünetmentes betegek pontosabb rizikóbecslései:
Több vizsgálat is zajlik jelenleg, amelyek megpróbálják a tünetmentes betegek azon csoportjait pontosan meghatározni, de a legtöbb plakk-analízissel kapcsolatos vizsgálat pl. ultrahang, a mindennapi klinikumban nem állja meg a helyét, a TCD és MRI vizsgálat elérhetősége (mind a vizsgálat mind az azt értékelő szempontjából) limitált. Több vizsgálat is bizonyította, hogy a tünetmentes betegek közül a nagyobb szűkülettel rendelkező betegeknél a legmagasabb a rizikója egy későbbi stroke-nak.
Napjainkban, néhány országban tünetmentes betegnél nem végeznek műtétet illetve a műtéti indikációt jelentő szűkület nagysága akár centrumokként is eltérő lehet (60-80% között).
5.1.4. Tünetmentes betegek szűrése
Populáció szintű szűrés nem javasolt, az előbbiekben említett alacsony prevalencia mellett (70%-os ACI szűkület 2% alatti előfordulása) nem gazdaságos.
5.1.5. Tünetmentes carotis stenosis olyan betegeknél, akik nem ér-, szívsebészeti műtétre várnak:
Nem tudtak összefüggést kimutatni az 50% illetve 70%-nál nagyobb tünetmentes ACI szűkületek és a perioperatív stroke-ok között. Az adatok azt mutatják, hogy feltehetően inkább kardiális eredetű embolizáció a felelős a perioperatív stroke-ok nagy részében, így a tünetmentes betegeknél perioperatív nyaki ultrahang és preventív carotis rekonstrukció nem indokolt.
5.2. Tünetes carotis stenosis
Tünetes carotis szűkületen az 50% feletti szűkületet értjük, amelynél a releváns oldali a. carotis ellátási területének (a. cerebri media) megfelelő stroke ill. TIA-nak megfelelő tünetek voltak 6 hónapon belül.
Jelenlegi tudásunk szerint a szélütés oka carotis szűkület esetén többségében a szűkületet okozó plakkból eredő embolizáció. Ennek eredete az apró plakk darabkák és/vagy az innen eredő apró thrombusok. Így nem meglepő, ha egy embolizáció történt, a közeljövőben nagy eséllyel történik egy következő. Tünetekként jellemzően olyan neurológiai góctüneteket várunk, amelyek az ACI ellátási régiójának megfelelő agyi területek egy meghatározott pontjának kiesésekor jelenhetnek meg.
FONTOS !!!!!
Carotis tünetek:
- kontralaterális monoparesis
- kontralateralis hemiparesis
- kontralateralis hemisensoropathia (paraeshesia)
- dysarthria
- dysphagia
- aphasia
- ipsilateralis amaurosis fugax vagy vakság
Nem carotis szűkületnek megfelelő tünetek:
- ájulás
- szédülés
- fülzúgás
- zavartság
- amnézia
5.2.1 A tünetektől eltelt idő szerepe
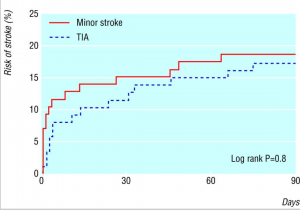
Két vizsgálat (NASCET és ECST) összevonásából készült, tünetes betegekre vonatkozó tanulmány hangsúlyozta a tünetektől eltelt idő fontosságát. Az újabb stroke bekövetkezésének rizikója az utolsó tünettől eltelt idővel exponenciálisan csökken. Egy TIA után 2 napon belül 5-8% a stroke bekövetkezésének esélye (ez a rizikó nagyjából megfelel a tünetmentes betegnél 10 év során összegyűlt rizikóval). Két hét alatt észlelt stroke ráta 11-25% volt. Ezért szerepel a legtöbb vezérfonalban ajánlásként, hogy lehetőleg a tünetes carotis szűkület a tünetektől számított két héten belül kerüljön műtétre.
Egymásnak ellentmondó adatokat lehet találni a tünetek után 48 órán belül – hyperacut – időszakban operált betegek eredményeiről. Egy svéd tanulmányban ebben az időszakban 11.5%-os stroke-rátát „sikerült” elérni, míg német és angol vizsgálatokban ugyanebben az időszakban (<48 óra) elvégzett endarterectomia során csak 3-3.7% volt.
Ábra – Újabb stroke rizikójának változása a tünet időpontjához viszonyítva
5.2.2. Szűkület mértékének, a nem és az életkor szerepe a műtéttel elérhető stroke prevencióban
- Tehát a 50-69% közötti carotis szűkületek esetén csak mérsékelt stroke ráta javulást lehetett elérni műtéttel.66
- Kisebb szűkületek esetén (0-30%) az ECST vizsgálat igazolta, hogy a műtéti kockázat stroke szempontjából magasabb, mint konzervatív terápia során észlelt stroke arány.
- A vizsgálatok többségében az életkor növekedésével a carotis endarterectomia rizikója nem emelkedett, azonban a carotis stenetelés során a perioperatív rizikó magasabb volt arányaiban az idősebb betegcsoportban.
5.2.3. Tünetes betegeknél választandó terápia
A nagyobb randomizált vizsgálatokban a carotis endareterctomiával jobb eredményeket lehetett elérni, mint a stent implantációval. A különböző betegcsoportokban az életkor, nem, ellenoldali elzáródás mind befolyásolta az eredményeket, csupán az ellenoldali elzáródás esetén és a 75 év alatti nőknél volt a carotis stentelés a műtéthez hasonló rizikójú beavatkozás, a többi esetben magasabb stroke ráta igazolódott.
5.2.4. Tünetes betegek kezelésének megítélése jelentős bénulás és instabil neurológiai állapot esetén
Mivel a carotis rekonstrukció célja a stroke rizikó csökkentése, olyan esetekben, ahol az ischemiás károsodás helyén vérzés intracerebralis vérzés léphet fel, nem javasolt a műtét elvégzése.
- Ilyen helyzet általában a jelentős bénulással járó esetek (módosított Rankin érték≥3)
- amikor az ischaemiás régió meghaladja az a. cerebri media ellátási területének harmadát
- amikor a beteg tudata jelentősen nem hozzáférhető, nem megítélhető.
Több olyan eset van, amikor a beteg a megfigyelésünk közben mutat ismétlődő vagy egyre rosszabbodó tüneteket. A „stroke in evolution” – kifejezéshez nincs pontos definíció, mivel minden stroke mutat az első időszakban, főleg az első pár órában, fluktuáló tüneteket. Általában olyan eseteket számítunk ide, amikor a meglévő tünetek rosszabbodnak. A crescendo TIA pedig olyan állapotot jelöl, amikor a betegnek egyre gyakrabban vannak tünetei, de azok tünetmentessé válnak 24 órán belül. Az instabil állapotban végzett rekonstrukciók valószínűleg magas, akár 10-20%-os stroke rizikóval járnak, mint azt pár közlemény is mutatja.
6. A beavatkozást végző centrum minőségi kritériumai
Fontos figyelembe venni, hogy a vizsgálatok, amelyekre hivatkozva a vezérfonalakat összeállítják, általában olyan centrumokban készülnek, ahol a magas beavatkozásszám mellett alacsony a perioperatív szövődmények száma. Általában elmondható, hogy olyan centrumban érdemes carotis rekonstrukciót végezni, ahol tünetmentes betegnél 3% alatti és tünetes betegeknél 6% alatti a perioperatív stroke ráta. Valószínüleg minimum 35 eset/év/kórház az az esetszám, amely alatt nem javasolt carotis rekonstrukciót végezni. A sebész által szükséges műtéti szám jelenleg nincs pontosan meghatározva, de évi 30 esetszám felett jobb eredményeket találtak. Ezen felül, javasolt, hogy érsebészek végezzenek carotis rekonstrukciót, mivel több országban más szakmák képviselői is végeznek ilyen műtéteket (pl. idegsebészek) igazoltan rosszabb eredménnyel.
7. Restenosis
Amennyiben a carotis rekonstrukció után 1-2 hónapon belül észlelnek a rekonstrukció területén szűkületet, azt inkább reziduális szűkületnek lehet nevezni. A neointimális hiperpláziából eredő visszaszűkülés általában 3-6 hónappal a rekonstrukció után szokott kezdődni. Amennyiben a beavatkozás után több mint 2 évvel észlelnek visszaszűkülést, az feltehetően atherosclerotikus eredetű.
Jelenleg nincs bizonyítva, hogy utánkövetés során észlelt restenosis magasabb ipszilaterális stroke aránnyal járna, mit azok a műtétek, amelyeknél nem észleltek visszaszűkülést. A műtét utáni szűrő jellegű ultrahang vizsgálat haszna kérdéses, stent implantáció után feltehetően nem szükséges, azonban evidencia erejű vizsgálatokra még szükség lenne ebben a kérdésben.
8. Dissectio
A carotis dissectió előfordulása stroke-on átesett betegek 2-3%-ában, (30 év alatti stroke-on átesett betegek körében 20% körüli az incidenciája) traumás sérülések esetén 1,2%-ban diagnosztizálják. Leggyakoribb tünet a nyaki fájdalom, fejfájás melletti stroke, TIA, egyoldali Horner-szindróma. Diagnosztikájánál a nyaki duplex UH vizsgálat érzékenysége alacsony, ezért a CTA, MRA esetlegesen DSA vizsgálat javasolt. Terápia során elsősorban konzervatív gyógyszeres kezelés (thrombocytaaggregáció gátlás, antikoaguláció) javasolt. Recidív tünetek esetében felmerül az intervenció során stent implantáció, azonban ennek szükségességéről az irodalmai adatok megoszlanak.
9. Aneurysma
Előfordulás: a perifériás érrendszerben kialakult aneurysmák 4%-a helyezkedik el az extracraniális carotis rendszerben. Általában tapintható pulzáló nyaki terime tünet miatt végzett UH vizsgálata kapcsán igazolódik. Ritkábban neurológiai tünetek, perifériás idegek és véna nyomás tünetei kapcsán kerül felfedezésre. Az első választandó diagnosztikai modalitás lehet az UH, ezt követően a műtéti kezelés tervezéséhez szükséges CTA vagy MRA végzése. Kezelése legtöbbször sebészi reszekció és reconstructio.
10. Tumor (carotistest tumor, chemodectoma, carotid body paraganglinoma)
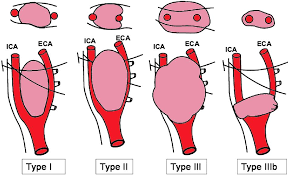
Több elnevezés is használatban van az elváltozással kapcsolatban: glomus caroticum paraganglioma, chemodectoma, valamint az angolszász területen leggyakrabban használt kifejezés a „carotid body tumor”. Neuroectoderma eredetű, lassan növekvő nyaki terime, általában 40-50 év közötti nőkön fordul elő. Mindkét oldalon a carotis bifurkáció belső oldalán az érfalban a media és az adventica között találhatóak a sejtek. Nem ritkán (10%) kétoldali az elváltozás. Az összes carotis-paraganglioma többségében (90%) jóindulatú és a növekedés hátterében nem sejtburjánzás, hanem a sejtek hipertrófiája figyelhető meg. Az elváltozás rosszindulatú, amennyiben a környező nyirokcsomókat és akár távoli szöveteket is érint. Hipervaszkularizált tumor, ezért a mintavétel nem javasolt szövettan céljából, mivel életet veszélyeztető vérzést okozhat. A diagnózis felállításához általában a képalkotó vizsgálatok elegendőek. A carotis-paraganglioma sebészi kezelése az esetek döntő többségében ajánlott. A rezekabilitás meghatározására a Shamblin-beosztás (I-III) javasolt, amely azt adja meg, hogy a tumor mennyire fonja körbe az ACI-t. A rezekció során nagy a vérveszteség, az ACI interpositum szükségességének és az agyi idegek sérülésének a lehetősége. A nagy vérveszteség csökkentésére többen javasolnak előzetes embolizációt. A betegek genetikai szűrése szukcinát-dehidrogenáz (SDH) –gén irányába javasolt, mivel azon betegeknél, ahol sikerül gén-mutációt bizonyítani évente javasolt nyaki ultrahangot végezni, családtagok szűrése illetve fej, nyak, mellkas has és kismedence MR vizsgálata is akár szóba jöhet.
carotis-paraganglioma Shamblin-beosztása
Összefoglalás
A nyaki verőérműtétek illetve a nyaki érszűkülettel kapcsolatos vizsgálatok egyértelmű célja a stroke megelőzése. Az ischaemiás szélütések közel 20%-ban az a. carotis interna elején lévő szűkületet lehet kórokként megjelölni. A lehetséges kezelések közül azt kell választani, amely mellett hosszabb távon lehet a stroke rizikóját csökkenteni. Ezt azért fontos hangsúlyozni, mert az invazív kezelésnek is van rizikójuk, a beavatkozás során illetve az azt követő rövid időszakban bekövetkezhet stroke, olyan, amely feltehetően az adott időszakban a beavatkozás nélkül nem alakult volna ki. Mivel a nyaki érszűkület az esetek többségében nem az áramlás csökkenésével, hanem a plakkból elszabaduló embolusok által okoz szélütést, a kezelést jelentősen befolyásolja, hogy a közelmúltban volt-e valakinek góctünete. Ezeknél a betegeknél sokkal magasabb a rizikója annak, hogy a pár napon, illetve 1-2 héten belül legyen egy újabb szélütés, amely esetleg olyan fokú lesz, hogy a beteg (és ezzel együtt a hozzá közel állók) életminőségét jelentősen befolyásolja. Ezekben az esetekben, hacsak a beteg egyéb megbetegedései miatt nincs a beavatkozásnak magas rizikója, a nyitott műtét, azaz az endarterctomia adja a legjobb eredményeket. A tünetmentes carotis stenosis kezelésében jelentős elmozdulás van BMT irányban, mert a gyógyszeres kezelés mellett alacsony stroke rizikót lehet elérni, amelynél a nyitott műtét illetve a stent implantáció csak 5-10 év elteltével kezd eredményesebb lenni. Stent implantáció elsősorban magas műtéti kockázatú betegeknél, restenosis és irradiált nyak esetén jár egyértelmű előnnyel, olyankor, amikor a műtéti feltárás jelentős kockázattal jár. Rendkívül fontos, hogy akár tünetes, akár tünetmentes esetekben olyan centrumban történjen a beavatkozás, ahol a perioperatív stroke ráta alacsony. Tünetmentes betegeknél a beavatkozás indikációja nem abszolút, az ideális terápia megválasztása egyéni szempontok alapján kell, hogy történjen, ahol a páciens életkora, neme, általános állapota, kísérőbetegségei, anatómiai sajátosságai és nem elhanyagolható mértékben a saját döntésének is szerepe kell, hogy legyen a döntéshozásban. Mivel nincs abszolút indikáció a tünetmentes betegcsoportban, éppen ezért más műtét kapcsán nincs létjogosultsága a preventív carotis rekonstrukciónak. A tünetmentes betegek szűrésére nincs szükség, azonban azoknál, akiknél a közelmúltban bénulás, pillanatnyi vakság, vagy bármilyen góctünet fordult elő szükség lenne a nyaki erek képalkotóval (Uh, CTA esetleg MRA) végzett vizsgálatára.