A szívizomzat vérellátásának akut megszűnése az infarktus során visszafordíthatatlan szöveti károsodáshoz és nekrózishoz vezet. Napjainkban a szívizom megmentésére a leghatékonyabb terápia a revaszkularizáció, amelyet vagy trombolízissel, vagy perkután koronária intervencióval (PCI), vagy koronária bypass (CABG) műtéttel végeznek. A véráramlás helyreállítása azonban további szövetkárosodáshoz vezethet. Ezt a jelenséget iszkémia/reperfúziós károsodásnak nevezzük, amely 4 módon jelentkezhet: az infarktusos szövet területének növekedése (lásd az 1. ábrát), megnövekedett mértékű mikrovaszkuláris obstrukció, ritmuszavarok nagyobb valószínűsége, csökkent szívkontraktilitás.
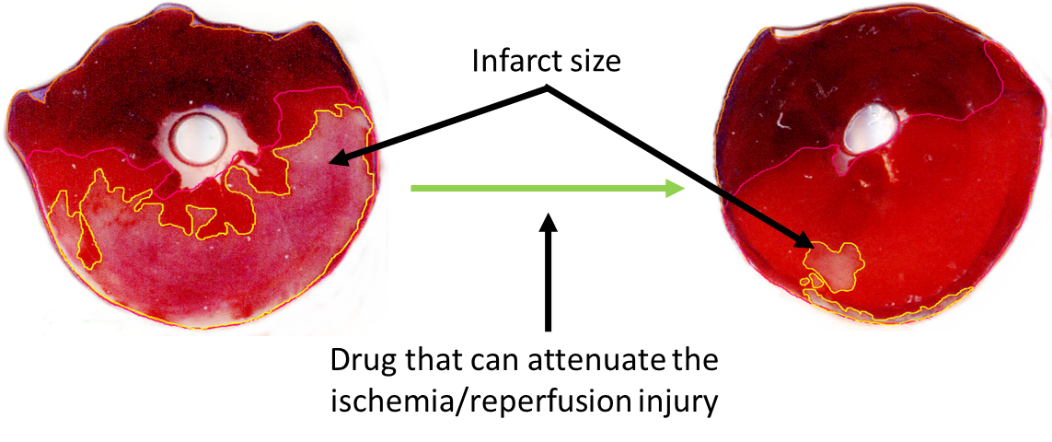
Az iszkémia/reperfúziós károsodás kezelésére még nem áll rendelkezésre engedélyezett gyógyszer, annak ellenére, hogy a területen nagyon intenzív kutatás folyik, azonban jelentős szükség lenne erre az infarktusos betegek akut és hosszú távú túlélésének és/vagy életminőségének javítása érdekében. A projektünkben a szív iszkémiás/reperfúziós sérülésének molekuláris aspektusait vizsgáljuk új farmakológiai célpontok azonosítása érdekében. Továbbá tanulmányozzuk az egyéb betegségek esetén alkalmazott hatóanyagok és az iszkémia/reperfúziós károsodás mértéke közötti kölcsönhatást (a gyógyszerek rejtett kardiotoxicitása), valamint a metabolikus betegségek hatását a kardioprotektív beavatkozásokra és kezelésekre.
1. A gyógyszerek hatása az iszkémia/reperfúziós károsodásra kisállatmodellekben: a rejtett kardiotoxicitás jelentősége
Projektvezetők: Dr. Görbe Anikó, Dr. Giricz Zoltán, Prof. Dr. Ferdinandy Péter
Projektfelelősök: Dr. Gergely Tamás, Bennet Weber, Nagy Regina
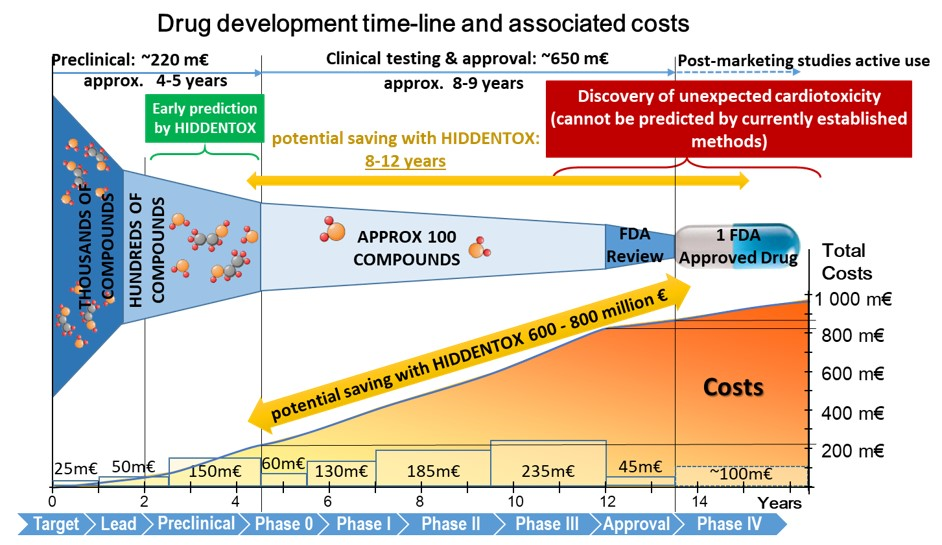
A nem várt szívre gyakorolt mellékhatások a klinikai vizsgálatok megszakításának és a gyógyszerek forgalomból való kivonásának legfőbb okai (lásd a 2. ábrát). A 90-es évek közepén végzett első megfigyelések óta jól ismert, hogy a kardiovaszkuláris kockázati tényezők és társbetegségek (mint például az öregedés, a hyperlipidaemia és a cukorbetegség), valamint az ezekre alkalmazott gyógyszerek (pl. nitrát-tolerancia, adenozin-trifoszfát-függő káliumgátló antidiabetikus gyógyszerek, sztatinok stb.) befolyásolhatják a szív iszkémiatűrését és az endogén kardioprotektív jelátviteli utakat. Ezen felül gyógyszerek hatóanyagai a beteg és kezelés alatt álló szívre olyan nemkívánatos hatásokat gyakorolhatnak, amelyek az egészséges szívizomban rejtve maradnak. A rejtett kardiotoxikus hatások hátterében (i) az iszkémia/reperfúziós sérülés és/vagy a rizikófaktorok jelenléte következtében kialakuló szövetkárosító jelátvitel útvonalak gyógyszerek által indukált felerősödése és/vagy (ii) a kardioprotektív túlélési jelátviteli utak gátlása állhat, amelyek iszkémia okozta sejthalálhoz és/vagy pro-aritmiás hatásokhoz vezethetnek. Így határoztuk meg a “rejtett kardiotoxicitás” új fogalmát, amely egy gyógyszer kardiotoxicitását jelenti, amely csak a beteg szívben jelentkezik, pl. iszkémiás/reperfúziós károsodással és/vagy a főbb társbetegségek jelenlétében. A rejtett kardiotoxicitás mechanizmusáról keveset tudunk, ráadásul nem mutatható ki a rutinszerűen alkalmazott, preklinikai, egészséges állatokon vagy szöveteken végzett szívbiztonsági vizsgálati módszerekkel. Ezért célunk a szívbetegségek (különösen a szívizom iszkémiája/reperfúziója és az iszkémiás kondicionálás) kombinált kísérleti in vivo és in vitro modelljeit tartalmazó új szívbiztonsági vizsgálati platform kifejlesztése a főbb szív- és érrendszeri társbetegségek és/vagy társkezelések jelenlétében és hiányában (Ferdinandy et al, European heart
journal, 2018).
Tanulási lehetőségek:
- irodalomkutatási módszerek,
- in vivo patkányvizsgálatok tervezése,
- kisállatok kezelése,
- szívműtétek elvégzése patkányokon,
- kvantitatív PCR és Western blotok elvégzése,
- az adatok kiértékelése és bemutatása.
Főbb publikációink a témában:
Ferdinandy, P. et al. Definition of hidden drug cardiotoxicity: paradigm change in cardiac safety testing and its clinical implications. Eur Heart J, 2018. (link)
Ferdinandy, P., et al. Interaction of risk factors, comorbidities, and comedications with ischemia/reperfusion injury and cardioprotection by preconditioning, postconditioning, and remote conditioning. Pharmacol Rev, 2014. 66(4): p. 1142-74. (link)
Brenner GB., et al. Hidden Cardiotoxicity of Rofecoxib Can be Revealed in Experimental Models of Ischemia/Reperfusion. Cells. 2020 Feb 26;9(3):551. (link)
Weber BY, et al. Rosiglitazone Does Not Show Major Hidden Cardiotoxicity in Models of Ischemia/Reperfusion but Abolishes Ischemic Preconditioning-Induced Antiarrhythmic Effects in Rats In Vivo. Pharmaceuticals (Basel). 2022 Aug 26;15(9):1055. (link)
Gergely TG, et al. Effects of Bempedoic Acid in Acute Myocardial Infarction in Rats: No Cardioprotection and No Hidden Cardiotoxicity. Int J Mol Sci. 2023 Jan 13;24(2):1585. (link)
2. Gyógyszerek hatása az iszkémia/reperfúziós károsodásra in vitro sejtkultúra modellekben
Projektvezető: Dr. Görbe Anikó
Projektfelelősök: Bennet Weber, Nagy Regina
Korábban bemutattuk, hogy a gyógyszerjelöltek biztonságosságát és rejtett kardiotoxikus hatását in vitro sejtkultúra-modellekben lehet vizsgálni, amelyekben az iszkémia/reperfúziós (I/R) károsodás és a társbetegségek szimulációja megvalósítható. A szívsejtvonalak és a primer izolált szívsejtek nagy áteresztőképességű gyógyszer-szűrésre használhatók, és alkalmazásuk előnyös a gyógyszerek szívsejtekregyakorolt közvetlen hatásainak felmérésére. Projektünkben olyan szereket tesztelünk, amelyek csak olyan társbetegségek, mint a hiperkoleszterinémia vagy az I/R károsodás jelenlétében mutathatnak közvetlen kardiotoxikus hatást a szívsejtekre.

Tanulási lehetőségek:
- irodalomkutatási módszerek,
- in vitro sejtkultúra alapú kísérletek tervezése,
- primer szívsejtek izolálása,
- sejtkultúrák fenntartása,
- a sejtek kezelése különböző hatóanyagokkal,
- sejtéletképességi vizsgálatok elvégzése,
- az adatok kiértékelése és bemutatása.
Főbb publikációink a témában:
Brenner GB., et al. Hidden Cardiotoxicity of Rofecoxib Can be Revealed in Experimental Models of Ischemia/Reperfusion. Cells. 2020 Feb 26;9(3):551. (link)
Weber BY, et al. Rosiglitazone Does Not Show Major Hidden Cardiotoxicity in Models of Ischemia/Reperfusion but Abolishes Ischemic Preconditioning-Induced Antiarrhythmic Effects in Rats In Vivo. Pharmaceuticals (Basel). 2022 Aug 26;15(9):1055. (link)
3. A szívre gyakorolt rejtett hatást mutató gyógyszerek által kiváltott transzkriptomikai változások vizsgálata
Projektvezető: Dr. Görbe Anikó
Projektfelelősök: Bennet Weber, Nagy Regina
Az endogén kardioprotektív folyamatok és molekulák jól ismertek a miokardiális iszkémia/reperfúziós (I/R) károsodás csökkentésében, amelyek hatásai gyakran elvesznek a klinikai transzláció során, különösen társbetegségek jelenlétében. Ezenkívül számos gyógyszer miokardiális mellékhatásokat/rejtett kardiotoxicitást mutathat, amelyre a jelenlegi gyógyszerfejlesztési gyakorlatban nem derül fény. A rejtett kardiotoxicitásban a génexpresszió változásai is szerepet játszhatnak, de ez jelenleg egy nem teljesen feltárt terület, és kutatásuk a biztonsági farmakológia új aspektusa. Projektünkben a szívizom mikroRNS és mRNS expressziós profilját kívánjuk vizsgálni egy bizonyítottan kardiotoxikus gyógyszerrel kezelt patkány akut I/R modellben, amely számos differenciálisan expresszálódó célmolekula felfedezését teszi lehetővé. A feltárt expressziós változások alapján azonosíthatók a mellékhatásokért felelős mechanizmusok is. A kiválasztott mikroRNS-ek potenciális toxikus vagy védő hatása validálható I/R rendszerben humán szívizomsejt modellben is. A bioinformatikai elemzés során előre jelzett molekuláris célpontok transzkript- és fehérjeszinten is validálhatók.
Tanulási lehetőségek:
- irodalomkutatási módszerek,
- in vitro sejtkultúra alapú kísérletek tervezése,
- sejtkultúrák fenntartása,
- a sejtek kezelése különböző hatóanyagokkal,
- miRNS célpont keresés és validálás kvantitatív PCR-rel és Western blottal,
- az adatok kiértékelése és bemutatása.
Főbb publikációink a témában:
Sághy É, et al. Cardiac miRNA Expression and their mRNA Targets in a Rat Model of Prediabetes. Int J Mol Sci. 2020 Mar 20;21(6):2128.




