Im Online-Core-Facility-System der Semmelweis Universität steht nun eine 3D-Bioprinting-Struktur zur Verfügung, die sowohl bei den akademischen Forschungen als auch bei der Kooperation mit industriellen Partnern anzuwenden ist. Die Forschungsarbeit im I. Institut für Pathologie und Experimentelle Krebsforschung wird von nun an mit einem 3D-Biodrucker – welcher Strukturen aus zuvor gezüchteten einzelnen Zellen herstellt -, sowie mit einem Gewebezüchter und Tierhaus unterstützt. Das System kann nicht nur der tumorbiologischen Grundlagenforschung im Institut helfen, sondern auch für Toxizitätstests von Medikamenten und Therapien, sowie für die personalisierte Therapie eingesetzt werden. Künftig sollen aus Tumorgewebe, das Patienten entnommen wurde, gedruckte Strukturen sogar zum Testen von Medikamenten und geplanten Behandlungen verwendet werden.
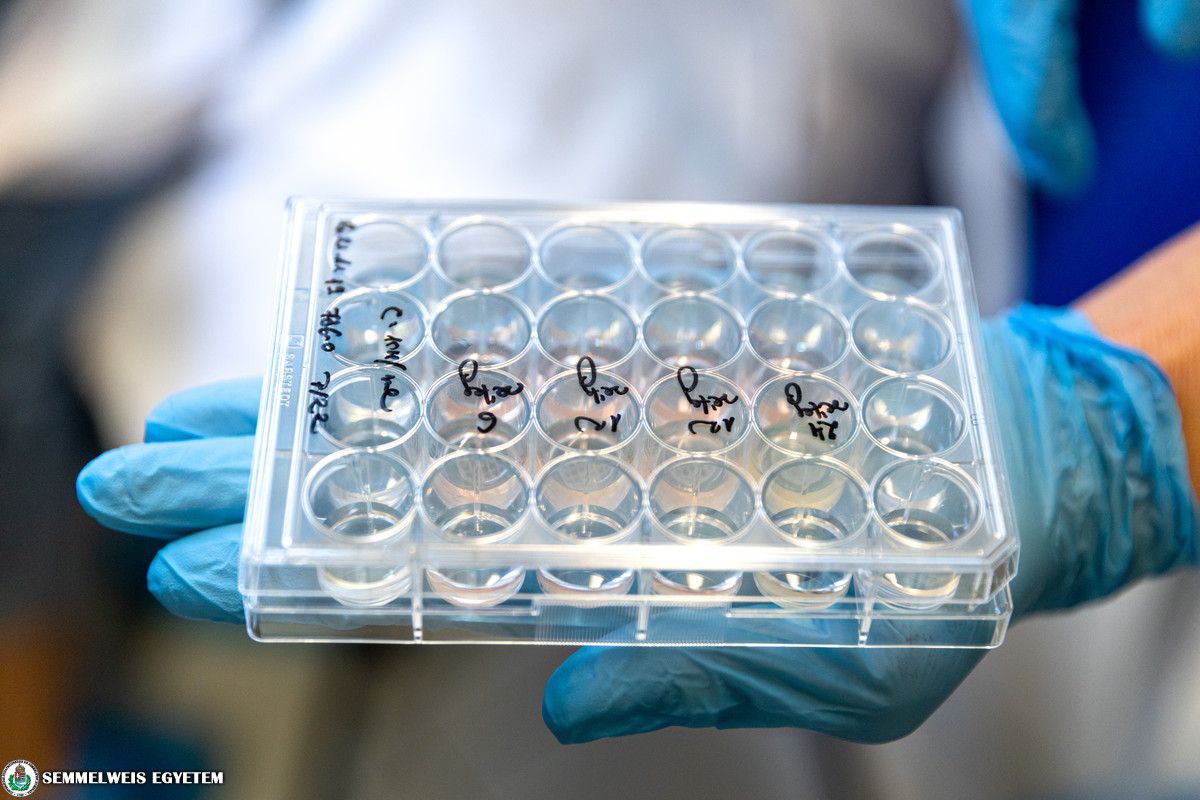
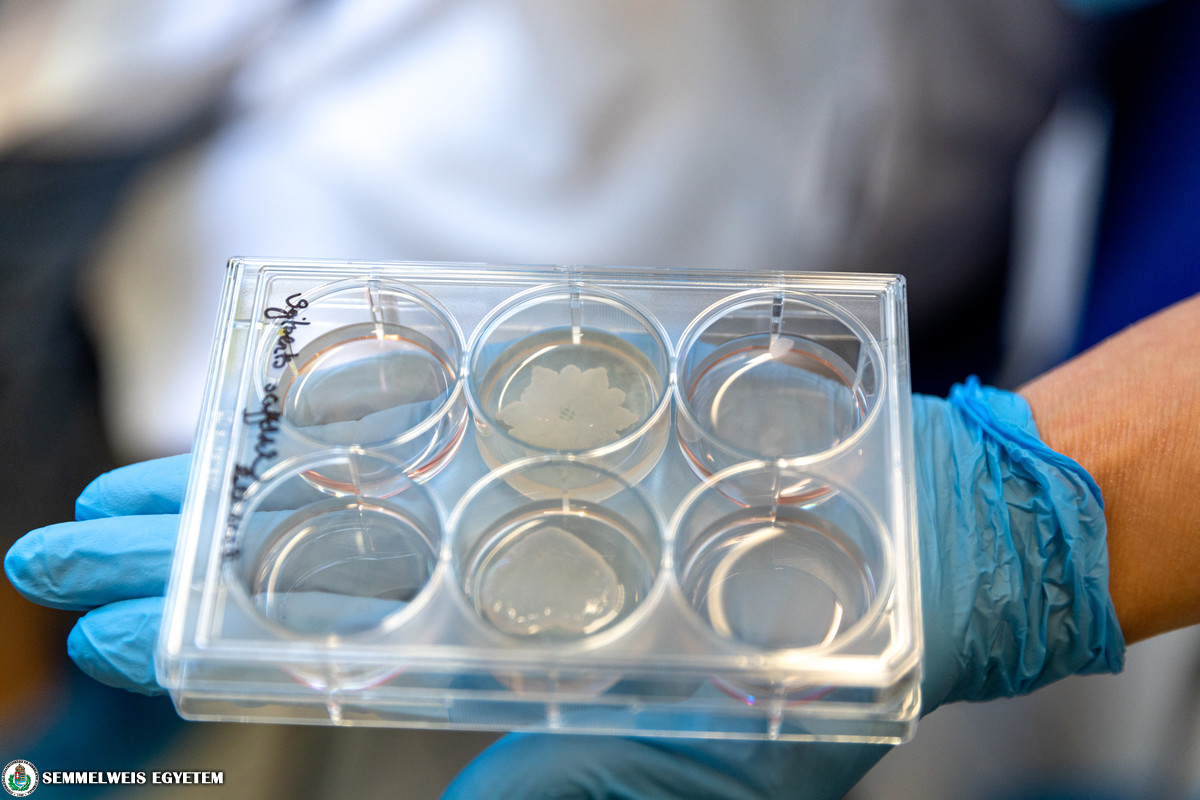
 Das tumorbiologische Laboratorium des I. Instituts für Pathologie und Experimentelle Krebsforschung befasst sich mit metabolischen Veränderungen in Tumoren und deren therapeutischer Hemmung. Mit Hilfe von Enzymen können Tumor- und andere Zellen aus Tumorproben, die in das Institut kommen, isoliert und dann mit einem gelartigen Matrixmaterial vermischt werden, um eine Biotinte für den 3D-Druck herzustellen. Das computergesteuerte Spezialgerät ist in der Lage, komplexe, gewebeähnliche Strukturen mit mehreren Biotinten gleichzeitig zu drucken. Das mikrometergenaue Biodrucken wird durch Druckluft unterstützt. Durch die Vernetzung des Matrixmaterials zwischen den Zellen kann die gedruckte Struktur so stabilisiert werden, dass die vorgegebene Form erhalten bleibt (z. B. Gefäßnetze, kleine Gewebescheiben, verschiedene Zellschichten usw.). Zu der ausgedruckten Struktur wird Nährlösung gegeben, und nach einigen Tagen oder sogar Wochen entstehen die gewebeähnlichen Modellen, die Zell-Zell-Kontakte bilden. Aus einem kleinen Stück Tumorgewebe sind Tumor- und andere Zellen in größerer Menge zu isolieren. So können aus Biotinte, die eine Tintenformulierung aus verschiedenen Zellen und Biomaterialien ist, viele kleine In-vitro-Gewebemodelle gedruckt werden. Diese Modelle können bei zahlreichen Untersuchungen benutzt werden: wie z.B. beim Testen von gezielten Behandlungen in Verbindung potentieller Antitumorwirkstoffe oder moderner molekulardiagnostischer Verfahren. Mithilfe der so erhaltenen Ergebnisse können nicht nur Projekte der Grundlagenforschung, sondern die präzisere Planung personalisierter Behandlungen unterstützt werden. Die Tests, die mit Hilfe des Druckverfahrens entwickelt werden, könnten die Entwicklung eines personalisierten Therapieplans mit ausgewählten Wirkstoffen für einen bestimmten Tumor ermöglichen. Mit der Diagnose könnte also auch der Therapieplan gleich erstellt werden. Zur Einführung dieses Verfahrens ist die Ausarbeitung von präzisen Protokollen nötig. Dazu werden gegenwärtig Untersuchungen mit tierischen Tumorgewebeproben durchgeführt. Daraufhin kann das Testen der Technologie bei Anwendung onkologischer Chirurgie beginnen.
Das tumorbiologische Laboratorium des I. Instituts für Pathologie und Experimentelle Krebsforschung befasst sich mit metabolischen Veränderungen in Tumoren und deren therapeutischer Hemmung. Mit Hilfe von Enzymen können Tumor- und andere Zellen aus Tumorproben, die in das Institut kommen, isoliert und dann mit einem gelartigen Matrixmaterial vermischt werden, um eine Biotinte für den 3D-Druck herzustellen. Das computergesteuerte Spezialgerät ist in der Lage, komplexe, gewebeähnliche Strukturen mit mehreren Biotinten gleichzeitig zu drucken. Das mikrometergenaue Biodrucken wird durch Druckluft unterstützt. Durch die Vernetzung des Matrixmaterials zwischen den Zellen kann die gedruckte Struktur so stabilisiert werden, dass die vorgegebene Form erhalten bleibt (z. B. Gefäßnetze, kleine Gewebescheiben, verschiedene Zellschichten usw.). Zu der ausgedruckten Struktur wird Nährlösung gegeben, und nach einigen Tagen oder sogar Wochen entstehen die gewebeähnlichen Modellen, die Zell-Zell-Kontakte bilden. Aus einem kleinen Stück Tumorgewebe sind Tumor- und andere Zellen in größerer Menge zu isolieren. So können aus Biotinte, die eine Tintenformulierung aus verschiedenen Zellen und Biomaterialien ist, viele kleine In-vitro-Gewebemodelle gedruckt werden. Diese Modelle können bei zahlreichen Untersuchungen benutzt werden: wie z.B. beim Testen von gezielten Behandlungen in Verbindung potentieller Antitumorwirkstoffe oder moderner molekulardiagnostischer Verfahren. Mithilfe der so erhaltenen Ergebnisse können nicht nur Projekte der Grundlagenforschung, sondern die präzisere Planung personalisierter Behandlungen unterstützt werden. Die Tests, die mit Hilfe des Druckverfahrens entwickelt werden, könnten die Entwicklung eines personalisierten Therapieplans mit ausgewählten Wirkstoffen für einen bestimmten Tumor ermöglichen. Mit der Diagnose könnte also auch der Therapieplan gleich erstellt werden. Zur Einführung dieses Verfahrens ist die Ausarbeitung von präzisen Protokollen nötig. Dazu werden gegenwärtig Untersuchungen mit tierischen Tumorgewebeproben durchgeführt. Daraufhin kann das Testen der Technologie bei Anwendung onkologischer Chirurgie beginnen.
In der Zellbank des Instituts stehen mehr als 200 humane Tumorzelllinien zur Verfügung. Wir haben mit Tests mit den aus Sicht der öffentlichen Gesundheit relevantesten Tumorzellen begonnen, und drucken gewebeähnliche 3D-Strukturen aus Brust- und Lungentumorzellen; außerdem testen wir das Drucken mit Darmkrebs- und Nierentumorzellen auch
– erklärte Dr. Anna Sebestyén, Senior Research Fellow des I. Instituts für Pathologie und Experimentelle Krebsforschung und Leiterin des Laboratoriums für Gewebe und Zellkulturen.
Zum Betreiben des 3D-Bioprinting-Laboratoriums sind ein professionelles Laboratorium für Gewebe und Zellkulturen sowie ein Tierhaus auch nötig – betonte die Forscherin. Im I. Institut für Pathologie und Experimentelle Krebsforschung stehen diese Mittel alle zur Verfügung. Die so aufgestellte Forschungsinfrastruktur steht sowohl für industrielle Kooperationen als auch für interne-externe akademische Kollaborationen zur Verfügung.
Neben Tumorforschung kann der 3D-Bioprinter in zahlreichen anderen Projekten angewendet werden: Die Pharma-, Lebensmittel- und Kosmetikindustrie kann damit zum Beispiel Toxizitätstests mit Hilfe der sogenannten Organ- oder Body-on-Chip-Modellen durchführen, die die Tierversuche ersetzen können. Bei diesen Modellen werden mithilfe des 3D-Bioprinters verschiedene Arten von lebendem Gewebe auf kleine Platten gedruckt. Die Hydratation, die Nährstoff- und Sauerstoffversorgung und die Aufrechterhaltung werden so gesichert, dass die Blutgefäße ebenfalls mit Modellierungsnetzen verbunden sind; und Toxizitätstests werden in dadurch entstandenen Modellen durchgeführt.
 Die Tumorbehandlung bedeutet ja eine große Herausforderung. Während den Eingriffen, der medikamentöser Behandlung und der Progression ändert sich das Tumor kontinuierlich. Die durch den 3D-Bioprinter hergestellten Geweben – ergänzt durch spezielle mikrofluidische Systeme – könnten in der Zukunft auch für Modellierung dieser Änderung benutzt werden. Anhand von langlebigen gewebeähnlichen 3D-Strukturen lässt sich untersuchen, wie ein aggressiver Tumorzellklon herausselektiert wird, und wie bestimmte Tumoren gegen eine Behandlung resistent werden. Neben den oben genannten sind die Vorteile der 3D-Modelle auch in der Arzneimittelentwicklung sinnvoll einzusetzen: unter solchen Umständen sind neue, potenzielle Krebswirkstoffe wirksamer als in den 2D-Zellkulturen zu testen. Selbstverständlich können diese neuartigen Versuche die endgültigen klinischen Studien und präventiven Tierversuche nicht ersetzen, aber sie können die Anzahl der erforderlichen Tierversuche und fehlgeschlagenen Phasenstudien verringern. Sie können ja dazu beitragen, die in Frage kommenden Wirkstoffe besser auszuwählen. Dadurch können die gegenwärtig hohen Kosten der Arzneimittelentwicklung in der Zukunft auch verringert werden – fügte die Forscherin dazu.
Die Tumorbehandlung bedeutet ja eine große Herausforderung. Während den Eingriffen, der medikamentöser Behandlung und der Progression ändert sich das Tumor kontinuierlich. Die durch den 3D-Bioprinter hergestellten Geweben – ergänzt durch spezielle mikrofluidische Systeme – könnten in der Zukunft auch für Modellierung dieser Änderung benutzt werden. Anhand von langlebigen gewebeähnlichen 3D-Strukturen lässt sich untersuchen, wie ein aggressiver Tumorzellklon herausselektiert wird, und wie bestimmte Tumoren gegen eine Behandlung resistent werden. Neben den oben genannten sind die Vorteile der 3D-Modelle auch in der Arzneimittelentwicklung sinnvoll einzusetzen: unter solchen Umständen sind neue, potenzielle Krebswirkstoffe wirksamer als in den 2D-Zellkulturen zu testen. Selbstverständlich können diese neuartigen Versuche die endgültigen klinischen Studien und präventiven Tierversuche nicht ersetzen, aber sie können die Anzahl der erforderlichen Tierversuche und fehlgeschlagenen Phasenstudien verringern. Sie können ja dazu beitragen, die in Frage kommenden Wirkstoffe besser auszuwählen. Dadurch können die gegenwärtig hohen Kosten der Arzneimittelentwicklung in der Zukunft auch verringert werden – fügte die Forscherin dazu.
Neben der intensiven Entwicklung molekularbiologischer und diagnostischer Techniken könnten die in den letzten Jahren verfügbar gewordenen Entwicklungen von In-vitro-Modellsystemen, einschließlich der 3D-Printer-Technologie, die zell- und tumorbiologischen Experimente zu Beginn des 21. Jahrhunderts revolutionieren. Dadurch erhält man neue Mittel zur weiteren Entwicklung der Präzisionsmedizin und der personalisierten Therapien – betonte Dr. Anna Sebestyén.
Ádám Szabó
Foto: Attila Kovács – Semmelweis Universität
Übersetzung: Judit Szlovák