A bélidegrendszer kísérletes és klinikai fejlődésbiológiai vizsgálata
A molekuláris és kísérletes embryológia napjaink egyik legdinamikusabban fejlődő tudományága, mely felhasználja a morfológia, a genetika, a molekuláris biológia és az őssejtbiológia eredményeit, módszereit. Az utóbbi években egyre nagyobb szerepet kaptak azok az embryomanipulációs és sejtjelölési kísérletek, amelyekben nyomon követhető egy őssejt eredete, vándorlása és differenciálódása. Fluoreszcens festékkel jelölt vagy a genetikailag módosított transzgenikus őssejtek transzplantációja alkalmas eszközt jelentenek annak meghatározására, hogy az izolált és visszaültetett őssejtek milyen szövetek, szervek kialakulásához járulnak hozzá.
A bélidegrendszer (enteric nervous system, ENS) a bélfalban található neuronokból és gliasejtekből álló kiterjedt hálózat, mely kritikus fontossággal bír a bélmotilitás regulációjában és a bélműködés egyéb alapvető vonatkozásaiban. A funkcionális gasztrointesztinális rendellenességek széles spektruma tartozik az ENS abnormalitások közé, ide soroljuk a Hirschsprung kórt (HSCR) is, aminek hátterében az enterális ganglionléc eredetű őssejtek bélben történő migrációjának zavar áll, s ami változó hosszúságú disztális intesztinális aganglionózishoz vezet. A jelenlegi kezelés az aganglionotikus vastagbél sebészi eltávolításából áll, azonban sok gyermek szenved a konstipációtól és az enterocolitistől. Az elmúlt évtizedben végzett őssejtkutatás felvetett annak a lehetőségét, hogy ezeket az enterikus neuronális ős/progenitor sejteket (enteric neuronal stem/progenitor cells-ENSCs) HSCR-ban szenvedő gyermekek kezelése során alkalmazzák, ebben a törekvésben mi is aktívan részt veszünk.
Madár, zebrahal és egér embryomanipulációs módszerekkel közel két évtizede kutatjuk az idegi-, vérképző-, mesenchymális-, és hám típusú embryonális és posztnatális őssejtek fejlődését, szöveti kölcsönhatását.
Címlapfotók korábbi munkáinkból:

Kutatási témák:
- ECM molekulák karakterizálása normál és a Hirschsprung-kór egérmodell szöveti környezetében.
Konkrét célkitűzéseink az alábbiak: (1) azonosítani az embrionális bél valamint a fejlődő enterikus ganglionléc sejtek által expresszált ECM-hoz asszociált faktorokat és (2) meghatározni mind ex vivo mind pedig in vivo körülmények között, hogy az ECM fehérjék, hogyan hatnak a posztnatális bélből izolált ENSC-ek migrációjára, proliferációjára és a differenciációjára. –in vitro szövetrekombináció, fluoromicrogyöngy beültetés embryoba, choriallantois membrán transzplantáció, velőcső átültetés ganglionléc őssejtek sorstérképezésére, embryonális kimérák készítése idegi és vérképző őssejtek nyomonkövetésére, parabiózis, RCAS-retrovírusos géntranszfekció, organoidok és idegi sejtaggregátumok ex vivo, in ovo, és in vivo transzplantációja embryokba, felnőtt és embryonális szervekbe, decelullarizált ECM „scaffoldok” manipulációja.
- Bélidegrendszerből izolált őssejtek differenciálódása embryonális és Hirschsprung-kór egérmodell szöveti környezetében.
Actb-DsRed és Wnt1-Cre:tdTomato transzgenikus egerek béltraktusából izolált idegi őssejtek tenyésztése során, „neurosphere” típusú idegi sejtaggregátumokat készítünk. A sejtaggregátumok fejlődési potenciálját korai embryokba történő transzplantációval teszteljük. Az embryonális fejlődés során megfigyelt migrációs és differenciálódási képesség vonásait összehasonlítjuk a felnőtt bélszövetbe történő differenciálódási képességgel.
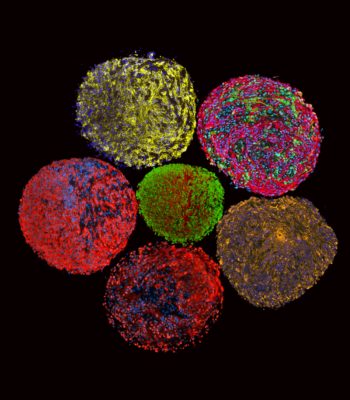
A kép különböző állatokból izolált neurosphereket ábrázol
- Embryonális bélidegrendszeri őssejtek izolálása és RNS szintű karakterizálása.
A vándorló bélidegrendszeri őssejtek transzkriptóm-analízise elengedhetetlenül szükséges, hogy megértsük és optimalizáljuk a sejtek vándorlását a neurointesztinalis betegségek gyógyításához szükséges őssejt-transzplantáció során. A kísérletek során a magas sejtvándorlási képességgel rendelkező, E11.5 Wnt1;tdT egérembrióból izolált kolonizáló ganglionléc-sejtek és a vándorlást befejező, nyugvó ganglionléc-sejtek RNSseq analízissel fényt próbálunk derítheti azokra a génekre amelyek a sejtek invazívítását szabályozzák. Ezzel lehetővé válna olyan új jelátviteli utak karakterizálása, melyek szerepet játszanak az embryonális és posztnatális idegsejtek vándorlásában.