Egy veseelégtelenséghez vezető kór, a nefrózis öröklődésével kapcsolatban számol be az eddigi gondolkodást jelentősen megváltoztató felismerésekről egy Nature Geneticsben most megjelent publikáció, melynek első szerzője dr. Tory Kálmán, a Semmelweis Egyetem I. Sz. Gyermekgyógyászati Klinikájának adjunktusa.
A Nature Genetics folyóiratban megjelent publikáció az I. Sz. Gyermekgyógyászati Klinika két akadémiai kutatócsoporttal (a klinikán működő, dr. Tulassay Tivadar vezette MTA-SE Gyermekgyógyászati és Nephrológiai Kutatócsoporttal, valamint a dr. Perczel András vezette MTA-ELTE Fehérjemodellező Kutatócsoporttal) és egy párizsi laborral (INSERM U983 laboratórium) együttműködésben végzett munkájának az eredménye.
 Dr. Tory Kálmán honlapunknak elmondta, a betegágy mellett tett megfigyelései adták a kutatás kiindulópontját, az ennek nyomán tett felismerések pedig szintén közvetlenül a gyakorlatban hasznosulnak. A gyermekgyógyász szakorvos arra figyelt fel, hogy ha a hagyományos (mendeli) öröklődés érvényesülne egy recesszív nefrózis szindrómában, akkor sokkal több ember kellene, hogy szenvedjen ebben a betegségben. Ennek okát keresve jutottak a most publikált új öröklésmenet felismerésére. Az eltérés hátterében eredményeik szerint ugyanis az áll, hogy ha mindkét szülő által hordozott gén-kópia is hibás, akkor sem lesz feltétlenül beteg a gyermekük, csak akkor, ha bizonyos hibák társulnak bizonyos hibákkal, nem mindegy ugyanis, hogy „ki kivel van párban”, vagyis milyen apai és milyen anyai hiba társul. „A társítások nagy részénél meg tudjuk mondani, hogy kórokiak-e vagy sem, így az eddig veszélyeztetettnek tartott szülőpárok nagy része fellélegezhet” – fogalmazott dr. Tory Kálmán, hozzátéve, hogy mindez megváltoztathatja a genetikai tanácsadást más recesszíven öröklődő betegségekben is.
Dr. Tory Kálmán honlapunknak elmondta, a betegágy mellett tett megfigyelései adták a kutatás kiindulópontját, az ennek nyomán tett felismerések pedig szintén közvetlenül a gyakorlatban hasznosulnak. A gyermekgyógyász szakorvos arra figyelt fel, hogy ha a hagyományos (mendeli) öröklődés érvényesülne egy recesszív nefrózis szindrómában, akkor sokkal több ember kellene, hogy szenvedjen ebben a betegségben. Ennek okát keresve jutottak a most publikált új öröklésmenet felismerésére. Az eltérés hátterében eredményeik szerint ugyanis az áll, hogy ha mindkét szülő által hordozott gén-kópia is hibás, akkor sem lesz feltétlenül beteg a gyermekük, csak akkor, ha bizonyos hibák társulnak bizonyos hibákkal, nem mindegy ugyanis, hogy „ki kivel van párban”, vagyis milyen apai és milyen anyai hiba társul. „A társítások nagy részénél meg tudjuk mondani, hogy kórokiak-e vagy sem, így az eddig veszélyeztetettnek tartott szülőpárok nagy része fellélegezhet” – fogalmazott dr. Tory Kálmán, hozzátéve, hogy mindez megváltoztathatja a genetikai tanácsadást más recesszíven öröklődő betegségekben is.
Mindez tehát azt jelenti, hogy a szerzők egy olyan genetikai polimorfizmust figyeltek meg, amelynek patogenitása a társuló mutáció függvénye: egyes mutációkkal betegséghez, míg másokkal „csendes” együttéléshez vezet. Hasonló ez ahhoz, mintha a klasszikus mendeli kísérletben egy gén négy allélját (A, B, C és D) vizsgálnánk, melyek közül kettő (A, B) homozigóta állapotban zöld, kettő (C, D) pedig sárga borsóhüvelyt eredményezne. A felfedezés az, hogy az A és B allél eltérő módon viselkedik a C és D alléllal szemben: míg az A mindkettővel szemben domináns, a B az egyikkel szemben recesszív viselkedést mutat (ábra). Ez a jelenség megváltoztathatja a humán genetikában a polimorfizmusok patogenitásának megítélését, az újonnan feltárt öröklésmenetnek köszönhetően ugyanis más gyakori polimorfizmus is lehet felelős ritka monogénes betegség megjelenéséért, ha az egy „megfelelő” mutációval társul.
 Mint az publikációról a magyar szerzők által készített, és honlapunknak elküldött összefoglalásban olvasható: a forradalmian új genetikai öröklésmenetet és annak következményeit a szerzők négy különböző szinten vizsgálták és bizonyították:
Mint az publikációról a magyar szerzők által készített, és honlapunknak elküldött összefoglalásban olvasható: a forradalmian új genetikai öröklésmenetet és annak következményeit a szerzők négy különböző szinten vizsgálták és bizonyították:
1) Epidemiológiai szinten rámutattak a klasszikus öröklésmenetből fakadó kockázat és a megfigyelt epidemiológiai tény ellentmondására, azaz a vizsgált polimorfizmus allélfrekvenciája és a betegség prevalenciája közötti eltérésre.
2) A francia laboratóriummal való kooperációban egyes családok példáján keresztül sikerült azonosítaniuk olyan egészséges családtagokat, akik a korábban patogénnek vélt genotípussal rendelkeznek, ám mégsem betegek.
3) A klinikai megfigyeléseket sikerrel igazolták sejtszinten, a vizsgált gén által kódolt podocin fehérje sejten belüli lokalizációjának vizsgálatával. Betegek vizeletéből tenyésztett podocyta sejteken és transzfektált podocyta-kultúrán kimutatták, hogy amennyiben a vizsgált polimorfizmus bizonyos mutációkkal társul, úgy a kódolt fehérje, a podocin nem jut ki a rendeltetési helyére, a sejtmembránba, és ez vezet a veseszűrő funkciójának sérüléséhez.
4) Végezetül az ELTE munkatársai, K. Menyhárd Dóra, Stráner Pál és Perczel András a genetikai módosulás következményét molekuláris-, sőt atomi-szinten, a podocin fehérje dimerképződési hajlamával korreláltatták és fehérje térszerkezetváltozással magyarázták a különböző polimorfizmus-mutáció párok eltérő hatását. A térszerkezetvizsgálat rámutatott arra, hogy a podocin fehérje „páralkotási” képességének megváltozása áll a jelenség hátterében. Amennyiben a két monomer egyikének szerkezetét a vizsgált polimorfizmus, míg a másikét a társuló specifikus mutációk valamelyike torzítja, a dimer szerkezete kóros lesz, és ez vezet a sejten belüli lokalizáció megváltozásához!
A munka kiemelkedő értéke a klasszikus öröklésmenet (mendeli szabályok) kiszélesítése mellett az, hogy a kutatás a tudományterületek szokatlanul széles körét ölelte fel. A gyakorló gyermekgyógyász betegágy mellett tett megfigyeléseiből kiindulva előbb a fehérje sejten belüli lokalizációjáig, majd annak térszerkezeti tulajdonságáig finomították a „képet”. A vizsgálatot végző kutatók örömére, a molekuláris szintű felismerések – a mikrokozmoszban megfigyelt molekuláris tulajdonságok és magyarázatok – azonnal és közvetlenül visszahatnak a genetikai tanácsadás, a gyakorló orvoslás szintjére.
A probléma komplex megközelítése magyar egyetemeken dolgozó kutatók és egy párizsi laboratórium intenzív együttműködésének eredménye, mely az ötletadó Bolyai-ösztöndíjas kutató, dr. Tory Kálmán gyermekgyógyász kitartó munkájának köszönhetően született meg. A vizsgált fehérjét kódoló gént másfél évtizeddel ezelőtt azonosító párizsi és a két hazai laboratórium sikeres együttműködése jól mutatja a határokon átívelő tudományban rejlő lehetőséget.
Dobozi Pálma
Fotó: Kovács Attila, Semmelweis Egyetem
Tory K, K Menyhárd D, Woerner S, Nevo F, Gribouval O, Kerti A, Stráner P, Arrondel C, Tulassay T, Mollet G, Perczel A, Antignac C: Mutation-dependent recessive inheritance of NPHS2-associated steroid-resistant nephrotic syndrome
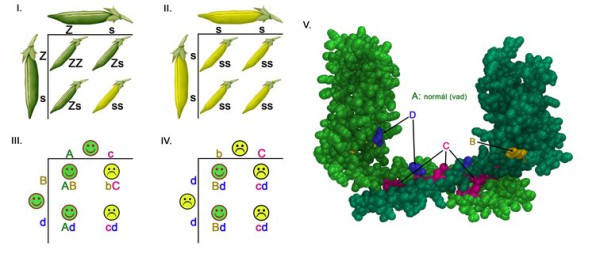
Ábramagyarázat:
A klasszikus és a mutáció-dependens autoszomális recesszív öröklésmenet közötti különbség
I-II.) A klasszikus mendeli öröklésmenet szerint a domináns fenotípusú, zöld hüvelyű borsók keresztezéséből legfeljebb 25% lehet a recesszív fenotípusú sárga hüvelyű borsók aránya (I.), illetve a recesszív fenotípusú sárga borsók keresztezéséből származó borsók mind sárgák (II.). (Z: domináns zöld fenotípust kódoló allél, s: recesszív sárga fenotípust kódoló allél)
III-IV.) Mutáció-dependens recesszív öröklésmenet esetén előfordulhat, hogy két domináns fenotípusú, egészséges (III.), illetve két beteg szülőnek (IV.) 50-50% eséllyel szülessen recesszív betegségben szenvedő gyermeke. Ennek oka, hogy a ‘B’ és a ‘C’ allélok domináns/recesszív karaktere a társuló allél függvénye. Míg a ‘B’ variáns a ‘C’ mutációval szemben recesszív karakterű (III., beteg gyermek ‘bC’ genotípussal), a ‘D’ mutációval szemben domináns (IV., egészséges gyermekek ‘Bd’ genotípussal). Hasonlóan, a ‘B’ alléllal szemben domináns ‘C’ allél a vad ‘A’ alléllal szemben recesszív (III., egészséges szülő ‘Ac’ genotípussal). [Homozigóta állapotban az ‘A’ és ‘B’ allélok egészséges (![]() ), a ‘C’ és ‘D’ allélok beteg fenotípust (
), a ‘C’ és ‘D’ allélok beteg fenotípust (![]() ) okoznak.]
) okoznak.]
V.) A podocin fehérje dimerjének térkitöltő modellje, ahol a vad ‘A’ allél által kódolt két monomer világos, illetve sötétzöld színű. A ‘B’, ‘C’ és ‘D’ betűk a III-IV. ábrán jelölt, ‘B’, ‘C’ és ‘D’ allélok által kódolt aminosav-változások helyét jelölik. A ‘B’ variáns azon (‘C’) mutációkkal patogén, melyek a dimerizációban szerepet játszó aminosavakat kódolják.


