|
Semmelweis Egyetem Budapest, Magatartástudományi Intézet/Semmelweis University, Institute of Behavioural Sciences Levelezési cím: H-1089 Budapest, Nagyvárad tér 4. E-mail: bodrob@net.sote.hu Absztrakt: Az élôvilágban megfigyelhetô prediktív homeosztázis a ritmikusan bekövetkezô környezeti változásokhoz való, elôrelátó adaptációt jelent. Ennek eklatáns példái a cirkadián ritmusok, amelyek a nappal és az éjszaka váltakozására készítik föl a szervezetet. A melatonintermelôdés cirkadián ritmusa anticipálja az alvásperiódus várható idôzítését és tartamát, az agyi ingerfeldolgozás alvásra jellemzô üzemmódját, továbbá – megfelelô környezeti feltételek mellett – az álmosság és részben az alvás megjelenését is elôsegíti. A melatonin alvásra gyakorolt hatásainak sajátosságai a lassú hullámú EEG-tevékenység csökkenése, illetve az alvási orsózásnak megfelelô EEG-tevékenység és a REM-alvás idejének fokozódása. Más hipnotikus hatású hatóanyagokhoz hasonlóan a melatonin is csökkenti a magtemperatúrát, de emellett számottevô kronobiotikus hatással is rendelkezik, amennyiben napszaktól függôen gyors és erélyes cirkadián fázisváltásokat képes elôidézni. Mivel a fény akutan gátolja a melatoninprodukciót, a megfelelô idôzítésû és alacsony hullámhosszú komponenseket is tartalmazó fény az exogén melatonin mellett, illetve azzal kombináltan felhasználható a jet-lag szindróma és más cirkadián ritmuszavarok kezelésében. Kulcsszavak: melatonin, alvás, cirkadián ritmusok, fényterápia, jet-lag, kronobiológia, kronoterápia, kronobiotikumok
Melatonin, sleep and the circadian rhythm: theoretical considerations and their chronopharmacological applications
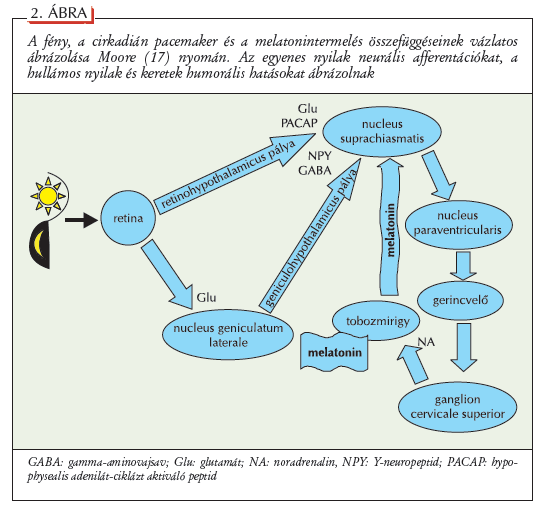
Abstract: The predictive homeostasis of living organisms is an anticipatory adaptation to rhythmical environmental changes. A good example for this is the circadian rhythm preparing the organism for the alternation of day and night. The circadian rhythm of melatonin production anticipates the timing and duration of nocturnal sleep of human subjects. It also induces a sleep-like stimulusprocessing mode of the brain and – in case of adequate environmental circumstances – a soporific and in part, a sleep-inducing effect. Specificities of melatonin effects on sleep are the reduction of slow-wave EEG activity, as well as the increase in seep EEG spindling and REM sleep time. Like other substances with hypnotic properties, melatonin decreases core body temperature, but has also a strong chronobiotic effect that is expressed as rapid and strong phase shifts of the circadian rhythm, depending on the time of day of melatonin administration. Because light acutely suppresses melatonin production, adequately timed light exposition, containing also low wavelength components, together with exogenous melatonin, could be useful in treating jet-lag syndrome and other circadian rhythm disorders. Keywords: melatonin, sleep, circadian rhythms, light therapy, jet-lag, chronobiology, chronotherapy, chronobiotics A homeosztázis az organizmusok és nyílt rendszerek sajátossága, amelynek révén a belsô környezetüket oly módon szabályozzák, hogy annak egy stabil állapotát, azaz az egyes paraméterek jellegzetes mintázatát tarthassák fönn. A fenti meghatározás Cannontól származik, aki a fogalmat a Test bölcsessége címû munkája keretében vezette be az élettanba (1). A belsô paraméterek állandóságát a változó környezetben biztosító mechanizmusoknak számos elônye van, ugyanakkor ezek a mechanizmusok költségesek és energiát igényelnek. Reaktív és prediktív homeosztázisA környezet némely lényeges paraméterének változása távolról sem tekinthetô véletlenszerûnek, hiszen a Föld saját tengelye körüli, illetve a Föld Nap körüli forgásából eredô georitmusok azt nagymértékben meghatározzák. A fényviszonyok váltakozása – bizonyos intenzitástartományokon belül – másodpercnyi pontossággal elôre jelezhetô. Kevésbé pontos, de hasonló „becslések” a hômérsékleti viszonyok tekintetében is tehetôk. A test bölcsessége – hogy Cannon megfogalmazásával éljünk – ezeknek a környezeti fluktuációknak az elôre látására is kiterjed, ez ugyanis hatékonyabb, mint utólag alkalmazkodni a változásokhoz. Prediktív homeosztázisnak nevezik azokat a mechanizmusokat, amelyek elôre látható környezeti változásokra készítik föl a szervezetet, mint amilyen a nappal és az éjszaka vagy az apály és a dagály váltakozása. E mechanizmusok közül a cirkadián ritmusokkal kapcsolatos folyamatok az élôvilágban széles körben elterjedtek, a nappal és az éjszaka váltakozásával összefüggô környezeti ingerekre készítik elô a szervezetet, és az ember esetében is rendkívüli jelentôségük van (2). Mindez kiegészül azokkal a kondicionált válaszokkal, amelyek a természetes és mesterséges környezetben tapasztalható ritmikus, napszakfüggô jelenségek, és a belsô fiziológiai paraméterek közötti társítások révén, mintegy részévé válnak a cirkadián fiziológiának. Mit anticipál a melatonintermelôdés?Régrôl ismert megfigyelés, hogy a fény gátolja a tobozmirigy melatonintermelését. Szakmai körökben is kevéssé ismert viszont, hogy a melatonin termelôdésében emellett cirkadián szabályozás is szerepet játszik, azaz állandó gyenge fényben követi a habituális napszakos aktivitás-nyugalom mintázatot: nappal nem termelôdik, éjszaka viszont folyamatos ébrenlét közben is intenzív felszabadulás veszi kezdetét, ami reggel, fény hiányában is alábbhagy, majd gyakorlatilag megszûnik (3). A melatonintermelés idejének azonban még ennél is pontosabb prediktív értéke van: a rövid és a hosszú alváshoz szoktatott kísérleti személyek melatoninprofilja „emlékszik” a habituális alvásidôre, és konstans alacsony intenzitású fény mellett a termelôdés idôtartamának formájában reprodukálja azt (3). Elég nagy bizonyossággal A melatonin központi idegrendszeri és alvásra gyakorolt hatásai ugyanakkor szintén a prediktív homeosztázis koncepciójába illeszkedô folyamatok, amennyiben alvásszerû munkamód irányába tolják el az ingerekre adott agyi válaszreakciókat. A funkcionális mágneses rezonanciával (fMRI) mért lokális agyi vérátáramlás-ingerek hatására tapasztalt csökkenése az úgynevezett negatív BOLD (blood oxygen level dependent – véroxigénszinttôl függô) -válaszként ismert jelenség, ami vélhetôen gátlás vagy diszfacilitáció eredménye. NREM alvásban az ébredési küszöb alatti intenzitással végzett vizuális és akusztikus ingerlés regionális agyi vérátáramlásban mérhetô csökkenést, azaz negatív BOLD-választ idéz elô (4, 5). Melatoninadagolást követôen, ébrenlétben vizsgált vizuális és akusztikus ingerlés hatására szintén negatív BOLD-választ, vagyis vérátáramlás-csökkenést figyeltek meg, méghozzá az alvás alatt is szignifikáns negatív BOLD-válasszal jellemezhetô agyi területeken (6). Ez a jelenség a NREM alvás egyik érdekes homeosztatikus tulajdonsága, és mintegy az ébresztôingerek elleni „alvásvédelmet” szolgálja. (Az ingerek paradox módon alvásvisszacsapást eredményeznek, nem ébredést.) Hasonló történhet melatonin hatására, ami az alvás munkamód felé tolja az agyi mûködéseket. A melatonin álmosító, illetve hipnotikus hatásai tekintetében az eredmények összetettnek mondhatók. Az exogén melatoninadagolás hatására a szubjektíven és EEG-vel (5,25–9 Hz-es teljesítmény) becsült, álmosságban bekövetkezô változások függenek például a vizsgálati alanyok testhelyzetétôl. Szignifikáns álmosságfokozódást mindkét mutató tekintetében csak fekvô testhelyzetben találtak, állóban nem (7). Ilyen elrendezésben viszont a melatonin csökkentette az alváslatenciát, akárcsak a melatonintermelés deficitjével jellemezhetô Angelman-szindrómában az alvás ideje alatt mért mozgások számát (8). Másfelôl az exogén melatonin álmosító hatásai elsôsorban az alacsony endogén melatoninprodukcióval jellemezhetô periódusokban érvényesül, vagyis akkor, amikor a tobozmirigy nem termel melatonint (9). A melatonin alvás-EEG-ujjlenyomata, vagyis az exogén melatonin hatására az alvás-EEG teljesítményspektrumában bekövetkezô változás jellegzetesnek mondható, amennyiben csökkent lassú hullámú aktivitás és fokozott alvási orsózásnak megfelelô szigma-teljesítmény jellemzi (10). Mindkét hatást leírták a benzodiazepinek esetében is (11), igaz a melatonin a benzodiazepinektôl eltérôen nem fokozza, inkább valamelyest még csökkenti is a béta-tevékenységet, ami kedvezôbb hatásprofilnak tekinthetô. Nagyobb dózisban (5 mg) a melatonin fokozza a REM alvásban töltött idôt is (10). Összegezve a fentieket, elmondható, hogy a melatonin anticipálja a napszak és a szervezetet korábban ért fény alapján várható alvásperiódust, e periódusban termelôdve pedig alvásszerû hatásokat, megfelelô körülmények között pedig fokozott álmosságot és alvást idéz elô. A cirkadián ritmusok és a melatoninAz endokrin mutatókban és a testhômérsékletben tetten érhetô napszakos ritmusok egy egységes cirkadián oszcillátor kimenetei és feed-back hurkai. Ennek a cirkadián pacemakernek van néhány kiemelten megbízható mutatója, amelyek a következôk: a melatoninszint, a kortizolszint és a magtemperatúra. Ezek akrofázisai azonos sorrendben éjszaka, reggel és délután mérhetôk (12). A melatoninfelszabadulás profilja egyrészt jellegzetesen éjszakai csúccsal és nappali minimummal jellemezhetô, ugyanakkor negatív összefüggésben áll az alvásperióduson belüli ébrenléttel és a magtemperatúrával: a magas melatonintermeléssel jellemezhetô idôszakok alacsony alvásperióduson belüli ébrenléttel és alacsony magtemperatúrával jellemezhetôk és viszont (10). A fenti összefüggések klinikai jelentôségét az adja, hogy a melatonin erôteljes hypothermiás hatásokkal jellemezhetô, ugyanakkor minden hipnogén hatóanyag (beleértve a benzodiazepineket, az etil-alkoholt, az általános anesztetikumokat és természetesen a melatonint is) egyben hypothermiás hatású is (13). Az akut hypothermiás hatások valószínûleg utánozzák a cirkadián elalvásszignált, de önmagukban nem biztosítják a kronobiotikus hatást. A benzodiazepinek között ugyanis egyaránt vannak kronobiotikus és nem kronobiotikus hatású vegyületek, amelyek eltérô mértékben befolyásolják a cirkadián ritmust, de hasonló hipnotikus hatásokkal jellemezhetôk (14). A melatonin kronobiotikus hatásai viszont erôteljesebbek a hagyományos hipnotikumok eddig feltárt kronobiotikus hatásainál.
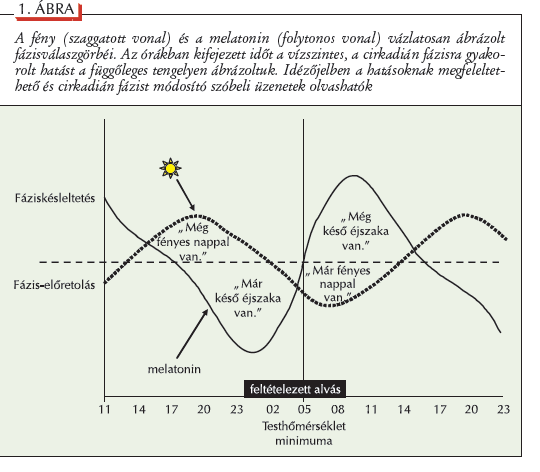
A fény és a melatoninMivel a csökkenô testhômérséklet és az alvásperióduson belüli alacsony ébrenléti idô az alvásminôség kedvezô feltételei, és mivel mindkettô a melatoninfelszabadulástól is függ, a melatoninprofil, illetve a melatonin cirkadián ritmusának fázisa kiemelten jelentôs az egészséges alvásmintázat szempontjából. A melatonin cirkadián ritmusának fázisát a fény igen erélyesen és rövid idô alatt képes befolyásolni. Ez egyaránt képezheti a deszinkronizált cirkadián ritmus reszinkronizációjának gyors és hatékony útját, és a fényszennyezôdés vagy még inkább a mesterséges világítás következtében kialakuló deszinkronizáció és alvászavar kiindulópontját. A fény nemcsak gátolja a melatonintermelést, hanem a cirkadián pacemakeren található melatoninreceptorokon keresztül a teljes cirkadián rendszer gyors fázisváltását is elôidézheti. A fény cirkadián ritmicitásra és melatoninprodukcióra gyakorolt hatása napszakfüggô. A nap közepén, a habituális ébrenlét periódusában, amikor a melatoninprodukció természetes módon is rendkívül alacsony, a fény nem befolyásolja a cirkadián ritmusokat. Az esti órákban, a habituális alvásperiódus közeledtével a fény gátolja a melatonintermelôdés cirkadián input következtében bekövetkezô termelôdését, ezáltal késôbbre tolva a melatoninprodukcióval jellemezhetô napszakot (1. ábra). Ez a cirkadián ritmus késleltetésének irányában történô fázisváltást jelent, ami annál nagyobb, minél késôbb éri fény a szervezetet és minél intenzívebb ez a fény. Könnyen belátható, hogy természetes körülmények között, nagyon magas szélességi köröktôl eltekintve, ennek a valószínûsége igen alacsony. A fény késleltetési hatása a szubjektív éjszaka közepéig érvényesül, ezen a ponton túl a szervezetet ért fény, bár szintén gátolja a melatonintermelôdést, de immár a siettetés irányába tolja a cirkadián ritmust (1. ábra), ami a következô estén tapasztalható, korábbi melatonintermelôdés formájában jut kifejezésre. A fentiek értelmében nem érdektelen megvizsgálni a fény melatoninszuppressziót okozó hatásának nemcsak a fázisválasz görbéjét, hanem a dózisfüggvényét is. A rendelkezésre álló adatok arra utalnak, hogy egy 500-1000 lux tartományba esô fényinger hatására hozzávetôlegesen 50%-os melatoninszuppresszió, míg egy 1000-3000 lux intenzitású fény hatására körülbelül 70%-os szuppresszió figyelhetô meg (3). A hatás azonban távolról sem lineáris, ezért a viszonylag alacsony intenzitású, beltéri világítás (~180 lux) is számottevô hatást gyakorolhat a cirkadián ritmicitásra (15). Ugyanakkor a fény hullámhossza is befolyásolja a hatást. A kis hullámhosszú (~450 nm) kék A fentiek figyelembevételével az idôzónák gyors átlépésekor jelentkezô jet-lag szindrómát gyorsabban és hatékonyabban lehet leküzdeni, ha az új idôzónába érkezéskor az utazó maga választhatja meg a természetes fényben tartózkodás idôszakát (20). Ennek az ajánlásnak a pontos részleteit a 3. ábra tartalmazza. Ehhez lényegében hasonló ajánlások más szakirodalmi forrásokban is megjelentek, azzal a különbséggel, hogy azokban a hat óránál nagyobb mértékû idôeltolódást követôen egy lépésben igyekszenek megoldani azt, ami az eredeti ajánlás szerint két fázisban optimális (21).
A sötétség és a melatonin kronobiotikus hatásaiTekintve, hogy a szubjektív éjszakának megfelelô periódusban melatonin termelôdik, és a melatonin erôteljesen befolyásolja a cirkadián fázisviszonyokat, a sötétség és a melatonin szintén rendelkeznek kronobiotikus hatásokkal. A délutáni sötétség képes fázis-elôretolódást elôidézni, ami az esti fény kronobiotikus hatásának a tükörképe (22). Mindez azonban feltételezi, hogy a cirkadián rendszer beindítja a melatoninprodukciót, ami többnyire csak a szubjektív éjszaka közeledtével válik lehetségessé. A direkt melatoninadagolás kronobiotikus hatásai ennél gyorsabb és erélyesebb fázismódosításokat is lehetôvé tesznek. A melatonin cirkadián rendszerre gyakorolt hatásának fázisválaszgörbéje a fény fázisválaszgörbéjének tükörképe: a délutáni-esti adagolás fázis- elôretolást (siettetést), a reggeli adagolás fáziskésleltetést idéz elô (1. ábra). Elôzô esetben biológiailag elôrehozzuk az éjszakát, utóbbiban pedig idôben kitoljuk. Ennek értelmében a melatonin kronobiotikumként való alkalmazásakor a fényterápiával ellentétes idôzítés javasolt. Egy átlagos felnôtt ember cirkadián ritmusát és fázisválaszgörbéjét figyelembe véve megfogalmazódott egy ajánlás, ami az átlépett idôzónák számának és az utazás irányának függvényében tartalmazza a melatoninbevétel javasolt idôpontjait (1. táblázat). Egy másik gyakorlat ezzel szemben azt látja célszerûnek, ha az új idôzóna szerinti esti órákban, egy órával a lefekvés elôtt nagyobb dózisú (3-5 mg) melatonint alkalmazunk az új éjszakai periódus konszolidációja céljából és a nagyobb dózisú melatonin álmosító hatásainak kihasználása révén. A melatonin természetesen fokozza a fényterápia kronobiotikus hatásait, fôleg a gyakorlatban nehezebben kivitelezhetô fázis-elôretolások esetén. Ilyenkor a délutáni-esti melatoninadagolást a reggeli-délelôtti fényterápiával ajánlott társítani (23).
A cirkadián ritmus fázisának meghatározásaA cirkadián ritmus fázisát gyenge fényben (~10 lux) félóránként mért melatoninszinttel lehet megállapítani. A DLMO (dim light melatonin onset – félhomályban mért melatonintermelôdés kezdete) a gátló fényhatás hiányában, cirkadián hatásra beinduló melatonintermelés kezdeti idôpontját adja meg. A 2 pg/ml plazmaszintnek megfelelô idôpont tekinthetô a biológiai éjszaka kezdetének. Ezt a mutatót – bár igen megbízható– becslésének költséges és körülményes volta miatt a klinikai gyakorlatban elvétve használják. A másik megbízható módszer a magtemperatúra minimumának megkeresése folyamatos monitorozással. Ez a mérés szintén körülményes, hiszen azt többek között a testmozgás és a táplálkozás is befolyásolja. A gyakorlatban ezért leggyakrabban az alvásnaplókra és a klinikai interjúkra támaszkodhatunk. A vizsgálatok összesített tapasztalata alapján elmondható, hogy a habituális, spontán ébredés idôpontja elôtt két órával mérhetô a magtemperatúra minimuma. Ugyanez a mutató éjszakai mûszakban dolgozó személyeknél, a szubjektív álmosság csúcsa alapján becsülhetô (9). Mindez átvezet a kronoterápiák kérdésköréhez, hiszen a spontán ébredés, illetve a szubjektív álmosság csúcsa alapján becsléseket tehetünk a késleltetett alvásfázis szindróma súlyossági fokának meghatározására. A korai ébredés és korai álmosság esetében pedig az elôretolt alvásfázis szindrómára vonatkozóan nyerhetünk információt. Más klinikai jelenségek, mint amilyen a nem 24 órás alvásébrenlét ciklus, az idôskori melatonindeficit vagy a melatoninhiánnyal járó Angelman-szindróma esetében ezek a mutatók még hasznosabbak lehetnek, hiszen itt a klinikai kép kevésbé egyértelmû, illetve idôben változó lehet.
|