A krónikus fogágy gyulladás és az Alzheimer-kór kapcsolata
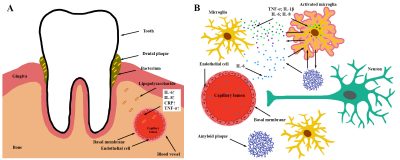 Az Alzheimer-kór a kognitív hanyatlás leggyakoribb oka, ami 50 millió embert érint világszerte, ugyanakkor kialakulásának pontos oka nem tisztázott. Az egyik uralkodó elmélet az úgynevezett gyulladásos hipotézis, miszerint a szervezetben lezajló krónikus gyulladás olyan módon változtatja meg az idegszövet működését, ami idegsejtelhalást okozhat. Ebben szerepe lehet a krónikus fogágy gyulladásnak (periodontitisz) is, ami a fogak támasztószöveteinek károsodásával jár, végül a fogak elvesztéséhez vezetve.
Az Alzheimer-kór a kognitív hanyatlás leggyakoribb oka, ami 50 millió embert érint világszerte, ugyanakkor kialakulásának pontos oka nem tisztázott. Az egyik uralkodó elmélet az úgynevezett gyulladásos hipotézis, miszerint a szervezetben lezajló krónikus gyulladás olyan módon változtatja meg az idegszövet működését, ami idegsejtelhalást okozhat. Ebben szerepe lehet a krónikus fogágy gyulladásnak (periodontitisz) is, ami a fogak támasztószöveteinek károsodásával jár, végül a fogak elvesztéséhez vezetve.
A demencia és a fogágy gyulladás közötti összefüggés nem kellőképpen tisztázott, mivel az eddig megjelent közlemények a gyulladás és a kognitív hanyatlás mértékének mérésére is rendkívül különböző módszertant alkalmaznak. Ennek eldöntésére tehát olyan kutatások szükségesek, amelyek egységes módon, kvantitatívan elemzik az ok-okozati kapcsolatot. Ugyanakkor amennyiben a két betegség közötti kapcsolat valóban fennáll, úgy feltételezhetően a demencia kialakulásának valószínűsége csökkenthető megfelelő szájhigiénia és fogászati kezelés alkalmazásával – összegezte dr. Bata Zsófia.
The Association of Periodontitis and Alzheimer’s Disease: How to Hit Two Birds with One Stone
Werber, Tom (Faculty of Medicine, Semmelweis University), Bata, Zsofia (Department of Conservative Dentistry, Semmelweis University), Vaszine, Eniko Szabo (Department of Conservative Dentistry, Semmelweis University), Berente, Dalida Borbala (Faculty of Medicine, Semmelweis University; Neurocognitive Research Center, National Institute of Mental Health, Neurology and Neurosurgery), Kamondi, Anita (Neurocognitive Research Center, National Institute of Mental Health, Neurology and Neurosurgery; Department of Neurology, Semmelweis University), Horvath, Andras Attila (Neurocognitive Research Center, National Institute of Mental Health, Neurology and Neurosurgery; Department of Anatomy, Histology and Embryology, Semmelweis University)
Journal of Alzheimer’s Disease, vol. 84, no. 1, pp. 1-21, 2021
doi.org/10.3233/JAD-210491
Gyulladásos útvonalak jelentősége a szívelégtelenség kórfolyamatában és kezelésében
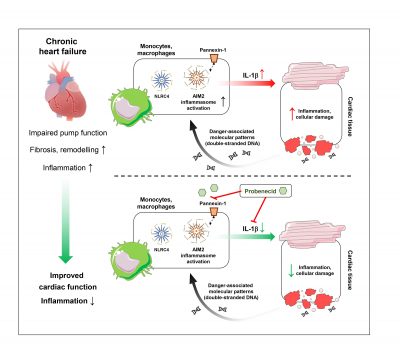 A krónikus szívelégtelenség kezelésében a transzplantáción és eszközös beavatkozásokon túl több gyógyszeres kezelési stratégia alkalmazható, azonban a betegség hosszútávon így is komoly fizikális, pszichés és anyagi terhet jelent a páciens és a társadalom számára egyaránt. Ismert, hogy a szívelégtelenség súlyosbodása mögött gyulladásos és immunológiai folyamatok is állnak, ugyanakkor jelenleg nincs a kórházi gyakorlatban olyan gyulladáscsökkentő gyógyszer, amely a szívelégtelenség kezelésében tartósan használatos lenne. Kutatásunkban szívelégtelen betegekből származó szívizom mintákon vizsgáltunk bizonyos gyulladásos folyamatokat, majd releváns állat- és sejtkultúramodelleken megerősítettük, hogy szívelégtelenség során az ún. AIM2 és NLRC4 inflammaszóma szenzorfehérjék mennyisége, valamint az általuk aktiválódó citokinek szöveti szintje megemelkedik emberben és patkánymodellben egyaránt. Az azonosított inflammaszóma aktivációt egy köszvény terápiában évtizedek óta sikerrel alkalmazott gyógyszerrel, probeneciddel gátoltuk krónikus szívelégtelenség patkánymodelljében. A probeneciddel kezelt állatok túlélése és szívfunkciója javult a kontroll állatokéhoz képest, és a gyulladáscsökkentő hatás is kimutatható volt.
A krónikus szívelégtelenség kezelésében a transzplantáción és eszközös beavatkozásokon túl több gyógyszeres kezelési stratégia alkalmazható, azonban a betegség hosszútávon így is komoly fizikális, pszichés és anyagi terhet jelent a páciens és a társadalom számára egyaránt. Ismert, hogy a szívelégtelenség súlyosbodása mögött gyulladásos és immunológiai folyamatok is állnak, ugyanakkor jelenleg nincs a kórházi gyakorlatban olyan gyulladáscsökkentő gyógyszer, amely a szívelégtelenség kezelésében tartósan használatos lenne. Kutatásunkban szívelégtelen betegekből származó szívizom mintákon vizsgáltunk bizonyos gyulladásos folyamatokat, majd releváns állat- és sejtkultúramodelleken megerősítettük, hogy szívelégtelenség során az ún. AIM2 és NLRC4 inflammaszóma szenzorfehérjék mennyisége, valamint az általuk aktiválódó citokinek szöveti szintje megemelkedik emberben és patkánymodellben egyaránt. Az azonosított inflammaszóma aktivációt egy köszvény terápiában évtizedek óta sikerrel alkalmazott gyógyszerrel, probeneciddel gátoltuk krónikus szívelégtelenség patkánymodelljében. A probeneciddel kezelt állatok túlélése és szívfunkciója javult a kontroll állatokéhoz képest, és a gyulladáscsökkentő hatás is kimutatható volt.
Eredményeink rámutatnak, hogy a gyulladáscsökkentő terápiák hatékonyak lehetnek krónikus szívelégtelenség kezelésében. Emellett felhívják a figyelmet a már piacon lévő gyógyszerek (pl. a probenecid) „újrahasznosításának” lehetőségére, az ún. gyógyszer újrapozícionálásra, amely a gyógyszerfejlesztés költséghatékonyabb és alkalmanként biztonságosabb formája lehet – fogalmazott összefoglalójában dr. Onódi Zsófia.
AIM2-driven inflammasome activation in heart failure
Zsófia Onódi (Department of Pharmacology and Pharmacotherapy, Semmelweis University), Mihály Ruppert (Heart and Vascular Center, Semmelweis University), Dániel Kucsera (Department of Pharmacology and Pharmacotherapy, Semmelweis University; HCEMM-SU Cardiometabolic Immunology Research Group), Alex Ali Sayour (Heart and Vascular Center, Semmelweis University), Viktória E Tóth (Department of Pharmacology and Pharmacotherapy, Semmelweis University; HCEMM-SU Cardiometabolic Immunology Research Group), Gábor Koncsos (Department of Pharmacology and Pharmacotherapy, Semmelweis University), Julianna Novák (Department of Pharmacology and Pharmacotherapy, Semmelweis University; HCEMM-SU Cardiometabolic Immunology Research Group), Gábor B Brenner (Department of Pharmacology and Pharmacotherapy, Semmelweis University; Pharmahungary Group; MTA-SE System Pharmacology Research Group, Department of Pharmacology and Pharmacotherapy, Semmelweis University), András Makkos (Department of Pharmacology and Pharmacotherapy, Semmelweis University; Pharmahungary Group; MTA-SE System Pharmacology Research Group, Department of Pharmacology and Pharmacotherapy, Semmelweis University), Tamás Baranyai (Department of Pharmacology and Pharmacotherapy, Semmelweis University), Zoltán Giricz (Department of Pharmacology and Pharmacotherapy, Semmelweis University; Pharmahungary Group), Anikó Görbe (Department of Pharmacology and Pharmacotherapy, Semmelweis University; Pharmahungary Group; MTA-SE System Pharmacology Research Group, Department of Pharmacology and Pharmacotherapy, Semmelweis University), Przemyslaw Leszek (Department of Heart Failure and Transplantology, Cardinal Stefan Wyszyński National Institute of Cardiology), Mariann Gyöngyösi (Department of Cardiology, Medical University of Vienna), Iván G Horváth (Heart Institute, Faculty of Medicine, University of Pécs), Iván G Horváth (Heart Institute, Faculty of Medicine, University of Pécs), Rainer Schulz (Institute of Physiology, Justus Liebig University Giessen), Béla Merkely (Heart and Vascular Center, Semmelweis University), Péter Ferdinandy (Department of Pharmacology and Pharmacotherapy, Semmelweis University; Pharmahungary Group; MTA-SE System Pharmacology Research Group, Department of Pharmacology and Pharmacotherapy, Semmelweis University), Tamás Radovits (Heart and Vascular Center, Semmelweis University), Zoltán V Varga (Department of Pharmacology and Pharmacotherapy, Semmelweis University; HCEMM-SU Cardiometabolic Immunology Research Group; Pharmahungary Group)
Cardiovascular Research, Volume 117, Issue 13, 15 November 2021, Pages 2639–2651. https://doi.org/10.1093/cvr/cvab202
Lymphoma terjedés vizsgálata multimodalitású képalkotás segítségével
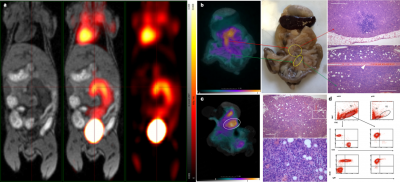 Az elmúlt évtizedekben az FDG PET/CT képalkotó módszer a tumor terápia hatékonyság becslésének legfontosabb eszközévé vált. Vizsgálataink során egerekben diffúz nagy B sejtes lymphomát (Bc-DLFL.1) vizsgáltunk, amely a humán agresszív lymphoma terjedésének modellje lehetett. Munkánkban választ kerestünk a radiofarmakonok sejtek általi felvételére, és az új Cserenkov-képalkotás (CLI) alkalmazhatóságára. Vizsgáltuk a radiofarmakonok szöveti eloszlásának inhomogenitását, mivel ismert, hogy ennek nagy jelentősége lehet a tumor prognózis becslésében és a kezelés tervezésében. A CLI egy olyan képalkotó módszer, amellyel számos a nukleáris medicina során használatos radiofarmakon nyomon követhető.
Az elmúlt évtizedekben az FDG PET/CT képalkotó módszer a tumor terápia hatékonyság becslésének legfontosabb eszközévé vált. Vizsgálataink során egerekben diffúz nagy B sejtes lymphomát (Bc-DLFL.1) vizsgáltunk, amely a humán agresszív lymphoma terjedésének modellje lehetett. Munkánkban választ kerestünk a radiofarmakonok sejtek általi felvételére, és az új Cserenkov-képalkotás (CLI) alkalmazhatóságára. Vizsgáltuk a radiofarmakonok szöveti eloszlásának inhomogenitását, mivel ismert, hogy ennek nagy jelentősége lehet a tumor prognózis becslésében és a kezelés tervezésében. A CLI egy olyan képalkotó módszer, amellyel számos a nukleáris medicina során használatos radiofarmakon nyomon követhető.
A cikkünkben bemutatunk és validálunk egy Cserenkov sugárzás alapú detektort. Eredményeink előrevetítik, hogy műtét közben gyorsan és hatékonyan ki tudjuk mutatni egy-egy alkalmazott radiofarmakon halmozódását. Ezáltal az tumor kivétele után azonnal vizsgálhatóvá válhat a sebészi szél érintettsége és a tumor inhomogenitása. Összességében a preklinikai vizsgálataink alapján támogatható a SPECT, a PET és a CLI együttes alkalmazása a klinikai onkológiai gyakorlatban is – írta összefoglalójában dr. Máthé Domokos.
In situ lymphoma imaging in a spontaneous mouse model using the Cerenkov Luminescence of F-18 and Ga-67 isotopes
Zsombor Ritter (Department of Nuclear Medicine, Medical School, University of Pécs), Katalin Zámbó (Department of Nuclear Medicine, Medical School, University of Pécs), Péter Balogh (Department of Immunology and Biotechnology, University of Pécs), Dávid Szöllősi (Department of Biophysics and Radiation Biology, Semmelweis University Faculty of Medicine), Xinkai Jia (Department of Immunology and Biotechnology, University of Pécs), Ákos Balázs (Semmelweis University Faculty of Medicine 1st Department of Surgery), Gabriella Taba (Semmelweis University Dosimetry and Medical Physics Service), Dániel Dezső (Department of Nuclear Medicine, Medical School, University of Pécs), Ildikó Horváth (Department of Biophysics and Radiation Biology, Semmelweis University Faculty of Medicine), Hussain Alizadeh (1St Department of Internal Medicine, University of Pécs Medical School), David Tuch (Lightpoint Medical Ltd.), Kunal Vyas (Lightpoint Medical Ltd.), Nikolett Hegedűs (Department of Biophysics and Radiation Biology, Semmelweis University Faculty of Medicine, CROmed Ltd.), Tibor Kovács (Institute of Radiochemistry and Radioecology, University of Pannonia), Krisztián Szigeti (Department of Biophysics and Radiation Biology, Semmelweis University Faculty of Medicine), Domokos Máthé (Department of Biophysics and Radiation Biology, Semmelweis University Faculty of Medicine, CROmed Ltd.; In vivo Imaging Advanced Core Facility, Hungarian Center of Excellence for Molecular Medicine (HCEMM)), Erzsébet Schmidt (Department of Nuclear Medicine, Medical School, University of Pécs)
Scientific Reports volume 11, Article number: 24002 (2021)
DOI: 10.1038/s41598-021-03505-3
Az ismétlődő negatív gondolkodás biológiája: az időperspektíva és a folátfogyasztás szerepe
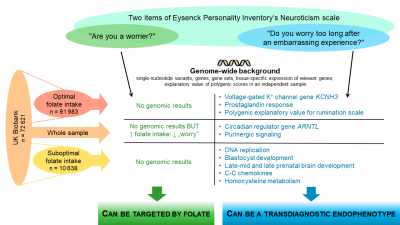 Az ismétlődő (perszeveratív) negatív gondolkodás számos testi és lelki betegségre (pl. depresszió, szorongás) hajlamosít, ezért biológiai meghatározóival is fontos tisztában lennünk. Mivel a folát nevű B-vitamin fogyasztása egész életünk során hatással lehet mentális működésünkre, jelen kutatásunkban az ismétlődő negatív gondolkodás két típusával való összefüggését vizsgáltuk középkorú felnőttek körében, kérdőíves módszerrel.
Az ismétlődő (perszeveratív) negatív gondolkodás számos testi és lelki betegségre (pl. depresszió, szorongás) hajlamosít, ezért biológiai meghatározóival is fontos tisztában lennünk. Mivel a folát nevű B-vitamin fogyasztása egész életünk során hatással lehet mentális működésünkre, jelen kutatásunkban az ismétlődő negatív gondolkodás két típusával való összefüggését vizsgáltuk középkorú felnőttek körében, kérdőíves módszerrel.
Eredményeink szerint az elégtelen folátbevitel az általános aggodalmaskodásra közvetlenül jelent kockázatot. Ezzel szemben egy múltbeli kínos eseményen való rágódás nem közvetlenül függ a folátbeviteltől, hanem a rá hajlamosító gének függnek tőle. Elégtelen folátbevitel esetén a DNS-osztódás, méhen belüli fejlődés és agyfejlődés, valamint az immunrendszer bizonyos génjei, elégséges folátbevitel esetén pedig agyi idegsejtek ingerelhetőségét, tanulékonyságát befolyásoló gének függnek össze a múlton való rágódással. Az összevont csoportban, folátbeviteltől függetlenül, pedig olyan, átfogó hatású gének függnek vele össze, amelyek hatással lehetnek mindezekre az eltérő folátérzékenységű biológiai részfolyamatokra – foglalta össze dr. Eszlári Nóra.
A cikk a Creative Commons „CC BY” licensze alapján jelent meg.
Biology of Perseverative Negative Thinking: The Role of Timing and Folate Intake
Nora Eszlari (Department of Pharmacodynamics, Faculty of Pharmacy, Semmelweis University; NAP-2-SE New Antidepressant Target Research Group, Hungarian Brain Research Program, Semmelweis University), Bence Bruncsics (Department of Measurement and Information Systems, Budapest University of Technology and Economics), Andras Millinghoffer (NAP-2-SE New Antidepressant Target Research Group, Hungarian Brain Research Program, Semmelweis University; Department of Measurement and Information Systems, Budapest University of Technology and Economics), Gabor Hullam (Department of Measurement and Information Systems, Budapest University of Technology and Economics; MTA-SE Neuropsychopharmacology and Neurochemistry Research Group, Hungarian Academy of Sciences, Semmelweis University), Peter Petschner (Department of Pharmacodynamics, Faculty of Pharmacy, Semmelweis University; MTA-SE Neuropsychopharmacology and Neurochemistry Research Group, Hungarian Academy of Sciences, Semmelweis University; Bioinformatics Center, Institute for Chemical Research, Kyoto University), Xenia Gonda (NAP-2-SE New Antidepressant Target Research Group, Hungarian Brain Research Program, Semmelweis University; MTA-SE Neuropsychopharmacology and Neurochemistry Research Group, Hungarian Academy of Sciences, Semmelweis University; Department of Psychiatry and Psychotherapy, Semmelweis University), Gerome Breen (Social, Genetic and Developmental Psychiatry Centre, Institute of Psychiatry, Psychology and Neuroscience, King’s College London; UK National Institute for Health Research (NIHR) Maudsley Biomedical Research Centre (BRC)), Peter Antal (Department of Measurement and Information Systems, Budapest University of Technology and Economics), Gyorgy Bagdy (Department of Pharmacodynamics, Faculty of Pharmacy, Semmelweis University; NAP-2-SE New Antidepressant Target Research Group, Hungarian Brain Research Program, Semmelweis University; MTA-SE Neuropsychopharmacology and Neurochemistry Research Group, Hungarian Academy of Sciences, Semmelweis University), John Francis William Deakin (Division of Neuroscience and Experimental Psychology, Faculty of Biology, Medicine and Health, The University of Manchester), Gabriella Juhasz (Department of Pharmacodynamics, Faculty of Pharmacy, Semmelweis University; MTA-SE Neuropsychopharmacology and Neurochemistry Research Group, Hungarian Academy of Sciences, Semmelweis University; SE-NAP 2 Genetic Brain Imaging Migraine Research Group, Hungarian Brain Research Program, Semmelweis University)
Nutrients 2021, 13(12), 4396.
https://doi.org/10.3390/nu13124396
Az affektív temperamentumok, illetve súlyos koszorúér-betegség kapcsolata
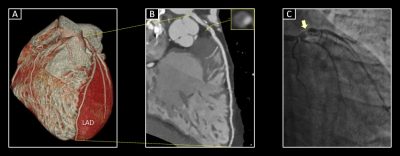 Az affektív temperamentumok (depresszív, ingerlékeny, szorongó, hipertím, ciklotím) olyan egyéni személyiségjegyek, jellemvonások összessége, melyek meghatározzák az egyén érzelmi reakciót adott helyzetekben. Ezen temperamentumok egyfelől bizonyos pszichiátriai kórképek előfutárainak tekinthetők, másrészt bizonyítottan emelik egyes szív- és érrendszeri betegségek kialakulásának rizikóját.
Az affektív temperamentumok (depresszív, ingerlékeny, szorongó, hipertím, ciklotím) olyan egyéni személyiségjegyek, jellemvonások összessége, melyek meghatározzák az egyén érzelmi reakciót adott helyzetekben. Ezen temperamentumok egyfelől bizonyos pszichiátriai kórképek előfutárainak tekinthetők, másrészt bizonyítottan emelik egyes szív- és érrendszeri betegségek kialakulásának rizikóját.
Keresztmetszeti vizsgálatunkba 225, a Városmajori Szív- és Érgyógyászati Klinikán klinikailag indikált koszorúér CTA-n átesett mellkasi panaszos beteget vontunk be. Eredményeink alapján mind az emelkedett koleszterin-szint, mind a gyakori hangulatingadozások által jellemzett ciklotím temperamentum növelik a súlyos fokú, stent beültetésének indikációját képző szűkületek jelenlétének valószínűségét. Másfelől viszont az optimista és extrovertált karakterjegyek által definiált hipertím temperamentum protektív hatásúnak bizonyult a súlyos fokú koszorúér-betegség tekintében a vizsgált populációban. Kutatásunk további evidenciát szolgáltat a temperamentumok kedvezőtlen prognosztikai szerepét illetően, rutinszerű alkalmazásuk tovább pontosíthatja a betegek egyéni szív- és érrendszeri rizikójának felmérését – fogalmazott összefoglalójában dr. Vecsey-Nagy Milán.
Association between affective temperaments and severe coronary artery disease
Milán Vecsey-Nagy (MTA-SE Cardiovascular Imaging Research Group, Heart and Vascular Center, Semmelweis University), Bálint Szilveszter (MTA-SE Cardiovascular Imaging Research Group, Heart and Vascular Center, Semmelweis University), Márton Kolossváry (MTA-SE Cardiovascular Imaging Research Group, Heart and Vascular Center, Semmelweis University), Melinda Boussoussou (MTA-SE Cardiovascular Imaging Research Group, Heart and Vascular Center, Semmelweis University), Borbála Vattay (MTA-SE Cardiovascular Imaging Research Group, Heart and Vascular Center, Semmelweis University), Xenia Gonda (NAP-2-SE New Antidepressant Target Research Group, Hungarian Brain Research Program, Semmelweis University; Department of Psychiatry and Psychotherapy, Semmelweis University; MTA-SE Neuropsychopharmacology and Neurochemistry Research Group), Zoltán Rihmer (Department of Psychiatry and Psychotherapy, Semmelweis University; Nyírő Gyula National Institute of Psychiatry and Addictions), Béla Merkely (MTA-SE Cardiovascular Imaging Research Group, Heart and Vascular Center, Semmelweis University), Pál Maurovich-Horvat (MTA-SE Cardiovascular Imaging Research Group, Heart and Vascular Center, Semmelweis University; Medical Imaging Centre, Semmelweis University), János Nemcsik (Department of Family Medicine, Semmelweis University; Health Service of Zugló (ZESZ))
Journal of Affective Disorders, Volume 295, 1 December 2021, Pages 914-919.
https://doi.org/10.1016/j.jad.2021.08.063
Makrofágok és a vér-bélidegrendszer gát kölcsönhatása a vastagbélgyulladásban
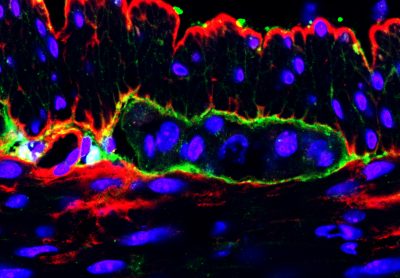
unit=micron
Kutatócsoportunk kutatási területe a bélhez-asszociált nyirokszervek és a bélidegrendszer fejlődése. Embryomanipulációs kísérletekkel, pár évvel ezelőtt kimutattuk, hogy a bélidegrendszer ganglionjaiban keringésből származó nyúlványos sejtek fordulnak elő. Az új sejttípust intraganglionáris makrofágoknak (IGM) neveztük el, ami az enterális neuronokat és gliát körbefonva, a ganglionokat környezetüktől elhatároló extracelluláris mátrix membránon belül helyezkednek el és kifejezetten a központi idegrendszeri microgliához hasonló markereket expresszálnak. Az IGM-et célzó vizsgálatokkal az enterális ganglionok körül található extracelluláris mátrix barrier szerkezetét és élettani funkcióját kívántuk megérteni. Szuper-rezolúciós és elektronmikroszkópiával kimutattuk, hogy a bélben létezik egy vér-bélidegrendszer gát, ami a vér-agy gáthoz hasonlóan folyamatos gliatalp rétegből, mátrix fehérjékből és bazális membránból áll.
Kísérleteink alapján a felnőtt egerek fluoreszcens dextránnal történt feltöltése információt nyújtott a vér-bélidegrendszer barrier permeabilitásáról, amit össze tudtuk hasonlítani a vér-agy gáttal. A fluorescens dextrán részecskék fagocitózisa alkalmas volt a makrofágok migrációjának in vivo követésére is. A makrofágok aktivitása és a barrier közötti kapcsolatot DSS-indukált egér bélgyulladásos modellben tanulmányoztuk, amit az liposzomális clodronate-al előidézett makrofág deplécióval ötvöztünk. Megállapítottuk, hogy colitis-ben a barrier lebomlik, permeabilitása megnő, kitéve a bélidegrendszer neuronjait a gyulladásos mikromiliőnek. Összefoglalva elmondható, hogy a bélidegrendszert határoló extracelluláris mátrix barrier normál és patológiás körülmények között érzékenyen reagál az intesztinális makrofágok jelenlétére és ennek kulcsszerepe van a bélidegrendszert érintő gyuladások patomechanizmusában – foglalta össze dr. Nagy Nándor.
Evidence of a Myenteric Plexus Barrier and Its Macrophage-Dependent Degradation During Murine Colitis: Implications in Enteric Neuroinflammation
David Dora (Department of Anatomy, Histology and Embryology, Faculty of Medicine, Semmelweis University), Szilamer Ferenczi (Institute of Experimental Medicine, Laboratory of Molecular Neuroendocrinology), Rhian Stavely (Department of Pediatric Surgery, Massachusetts General Hospital, Harvard Medical School), Viktoria E. Toth (Department of Pharmacology and Pharmacotherapy, Semmelweis University; HCEMM-SU Cardiometabolic Immunology Research Group, Semmelweis University), Zoltan V. Varga (Department of Pharmacology and Pharmacotherapy, Semmelweis University; HCEMM-SU Cardiometabolic Immunology Research Group, Semmelweis University), Tamas Kovacs (Department of Anatomy, Histology and Embryology, Faculty of Medicine, Semmelweis University), Ildiko Bodi (Department of Anatomy, Histology and Embryology, Faculty of Medicine, Semmelweis University), Ryo Hotta (Department of Pediatric Surgery, Massachusetts General Hospital, Harvard Medical School), Krisztina J. Kovacs (Institute of Experimental Medicine, Laboratory of Molecular Neuroendocrinology), Allan M. Goldstein (Department of Pediatric Surgery, Massachusetts General Hospital, Harvard Medical School), Nandor Nagy (Department of Anatomy, Histology and Embryology, Faculty of Medicine, Semmelweis University)
CMGH, Vol. 12, Issue 5, pp. 1617-1641. 2021
DOI: https://doi.org/10.1016/j.jcmgh.2021.07.003
A HIV-fertőzés indirekt módon gyorsíthatja a koszorúér-betegség progresszióját. Egy longitudinális vizsgálat eredményei.
Régóta ismert, hogy a HIV-fertőzöttek körében gyakoribbak a nemkívánatos kardiovaszkuláris események, úgy mint a szívinfarktus. Az elmúlt évtizedben egyes eredmények kimutatták, hogy HIV-fertőzöttek körében több a nem-kalcifikált vulnerábilis plakk, amely magyarázhatja a megnövekedett rizikóját ezen betegeknek, mivel ezek később okozhatnak nemkívánatos kardiovaszkuláris eseményeket. Azonban nem ismert, hogy pontosan milyen mechanizmusok álnak ezen jelenség hátterében.
Egyes vizsgálatok kimutatták, hogy a HIV-fertőzés függetlenül megnöveli a nem-kalcifikált vulnerábilis plakkok számát, amely azt jelenti, hogy ezen betegeknek mindenképp rosszabb koszorúér-státuszuk lesz mint hasonló nem fertőzött társuknál. Azonban a mi longitudinális vizsgálatunk rámutatott, hogy valószínűbb, hogy a HIV potencírozza a többi rizikófaktor negatív hatását, így ha szigorúbb kontroll alatt tartjuk a rizikófaktorokat, akkor elkerülhető lehet a HIV negatív hatása a koszorúér-betegségre – foglalta össze dr. Kolossváry Márton.
HIV indirectly accelerates coronary artery disease by promoting the effects of risk factors: longitudinal observational study
Márton Kolossváry (Department of Pathology, Johns Hopkins University School of Medicine; MTA-SE Cardiovascular Imaging Research Group, Heart and Vascular Center, Semmelweis University), David Celentano (Department of Epidemiology, Johns Hopkins University Bloomberg School of Public Health), Gary Gerstenblith (Department of Medicine, Johns Hopkins University School of Medicine), David A. Bluemke (School of Medicine and Public Health, University of Wisconsin), Raul N. Mandler (National Institute on Drug Abuse, National Institutes of Health), Elliot K. Fishman (Department of Radiology, Johns Hopkins University School of Medicine), Sandeepan Bhatia (Institute of Human Virology, University of Maryland School of Medicine), Shaoguang Chen (Institute of Human Virology, University of Maryland School of Medicine), Shenghan Lai (Department of Pathology, Johns Hopkins University School of Medicine; Department of Epidemiology, Johns Hopkins University Bloomberg School of Public Health; Department of Medicine, Johns Hopkins University School of Medicine; Department of Radiology, Johns Hopkins University School of Medicine; Institute of Human Virology, University of Maryland School of Medicine), Hong Lai (Department of Radiology, Johns Hopkins University School of Medicine; Institute of Human Virology, University of Maryland School of Medicine)
Scientific Reports 11, 23110 (2021).
https://doi.org/10.1038/s41598-021-02556-w
A rövid összefoglalókat a tudományos publikációk szerzői készítették.
Szerkesztette: Szabó Ádám
Fotó: a publikációkból származó képek
A cikket a Semmelweis Egyetem Kommunikációs Igazgatósága tette közzé.
