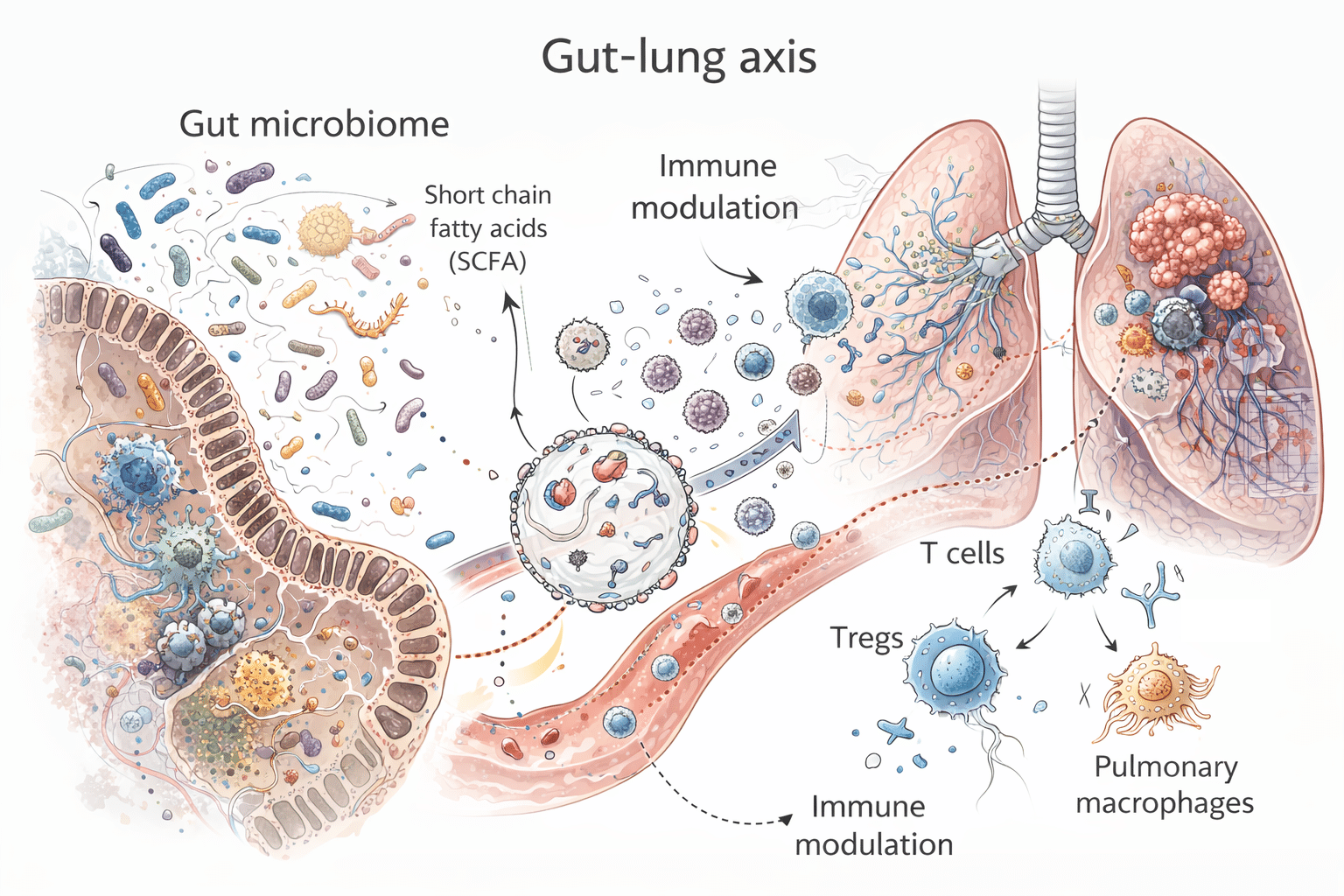Tartalomjegyzék:
- Tumor mikrokörnyezet feltérképezése in situ technikákkal tüdőrákban
- A bél mikrobiom hatása a tumorellenes immunitásra és az immunterápiára
- Eszközök, módszerek
Tumor mikrokörnyezet feltérképezése in situ technikákkal tüdőrákban
A tüdőrák és annak leggyakoribb változata, a nem kissejtes tüdőrák (NSCLC), továbbra is az egyik vezető halálok a daganatos betegségek között világszerte. Az immunterápiák, különösen az immunellenőrzőpont-gátlók (ICI) terén elért előrelépések ellenére a jelenlegi kezelések hatékonysága korlátozott, és a meglévő biomarkerek, mint a PD-L1 expresszió és a tumor mutációs terhelése (tumor mutation burden, TMB) prediktív ereje nem kielégítő. A kutatási projekt célja olyan új szöveti biomarkerek felfedezése, amelyek jobban meg tudják jósolni, hogyan reagál egy beteg az immunterápiára.
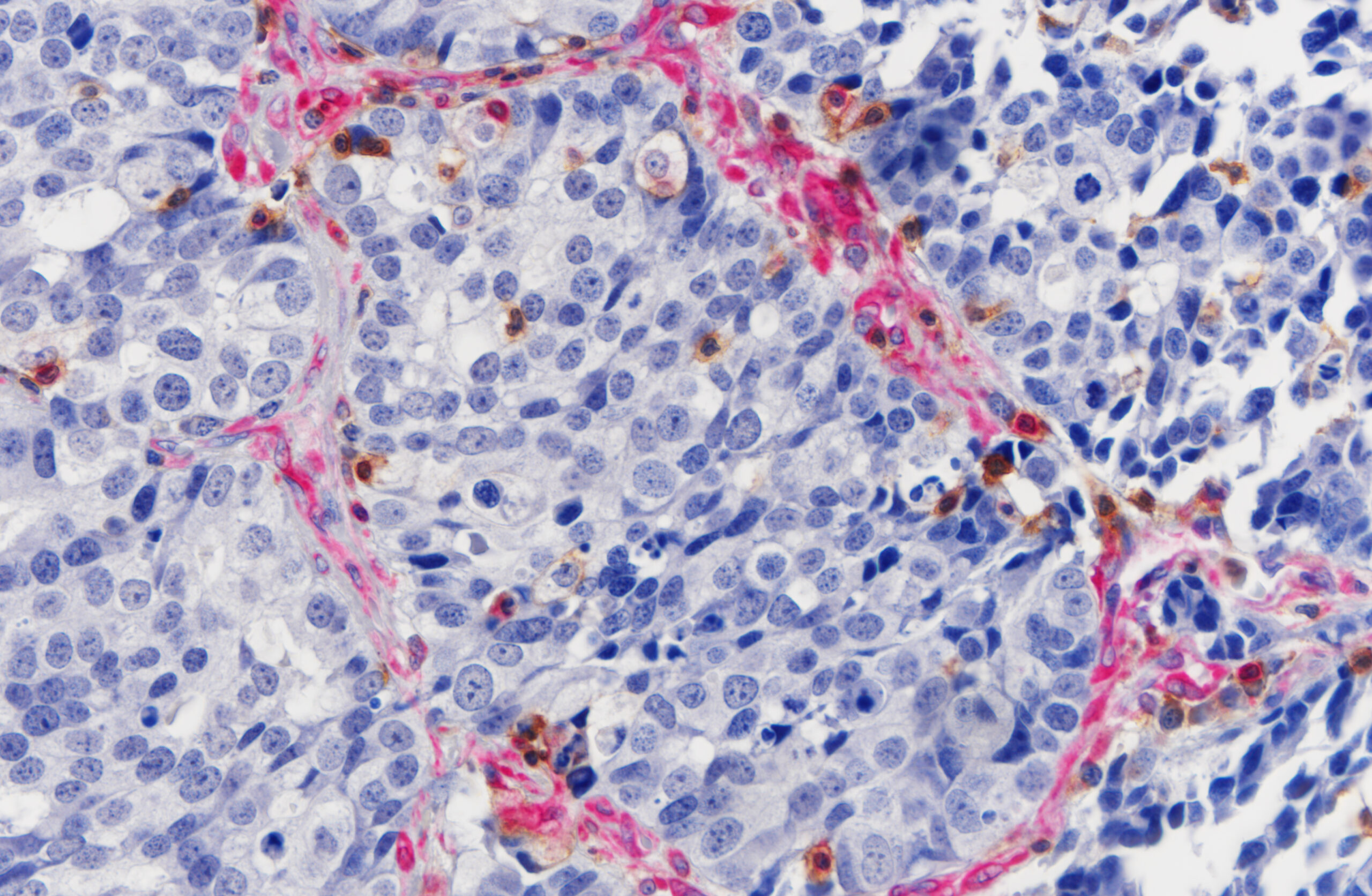
Az elmúlt évtizedben a daganatok mikro-környezete (tumor micro-environment, TME) a daganatbiológia egyik legfontosabb részévé vált. A tudományos adatok szoros kapcsolatot mutatnak bizonyos immunsejt-populációk intratumorális sűrűsége és a betegek túlélése és terápiás válasza között. A CD8+ citotoxikus T-sejtek a tumorellenes védekezés fő végrehajtói, mivel specifikusan támadják a tumorsejteket, hosszú távú védelmet biztosítva. A veleszületett immunsejtek (ILC-k) közvetlenül és közvetetten is szabályozzák a TME-t, míg az NK sejtek és a γδ T-sejtek közvetlenül pusztítják a tumorsejteket. A Treg-ek, az MDSC-k és az M2-szerű TAM-ok pedig pro-tumor hatású immunsejtek. A CD8+ T-sejtek infiltrációját a TAM-ok és Treg-ek is befolyásolják, amelyek a tumorsejtek túlélését és proliferációját segíthetik. A T-sejtek azonban hajlamosak kimerülni az immunszuppresszív TME-ben, így a sejtsűrűség és arányok nem mindig tükrözik hűen a daganatellenes immunválaszt. Az immun-ellenörzőpontok (immune-checkpoints, PD-L1, CTLA-4) és a CD8+ T-sejteken található kimerültségi (exhaustion) markerek (PD1, LAG3, TIM3, TIGIT) további értékes információkat nyújthatnak a tumor immun-környezetéről.
A projekt központi céljai:
- Rendelkezésre álló retrospektív és prospektív tüdőtumoros (nem-kissejtes tüdőrák, NSCLC és kissejtes tüdőrák, SCLC) betegcohortok formalin-fixált, paraffinba beágyazott mintáiból tissue microarray (TMA)-k készítése
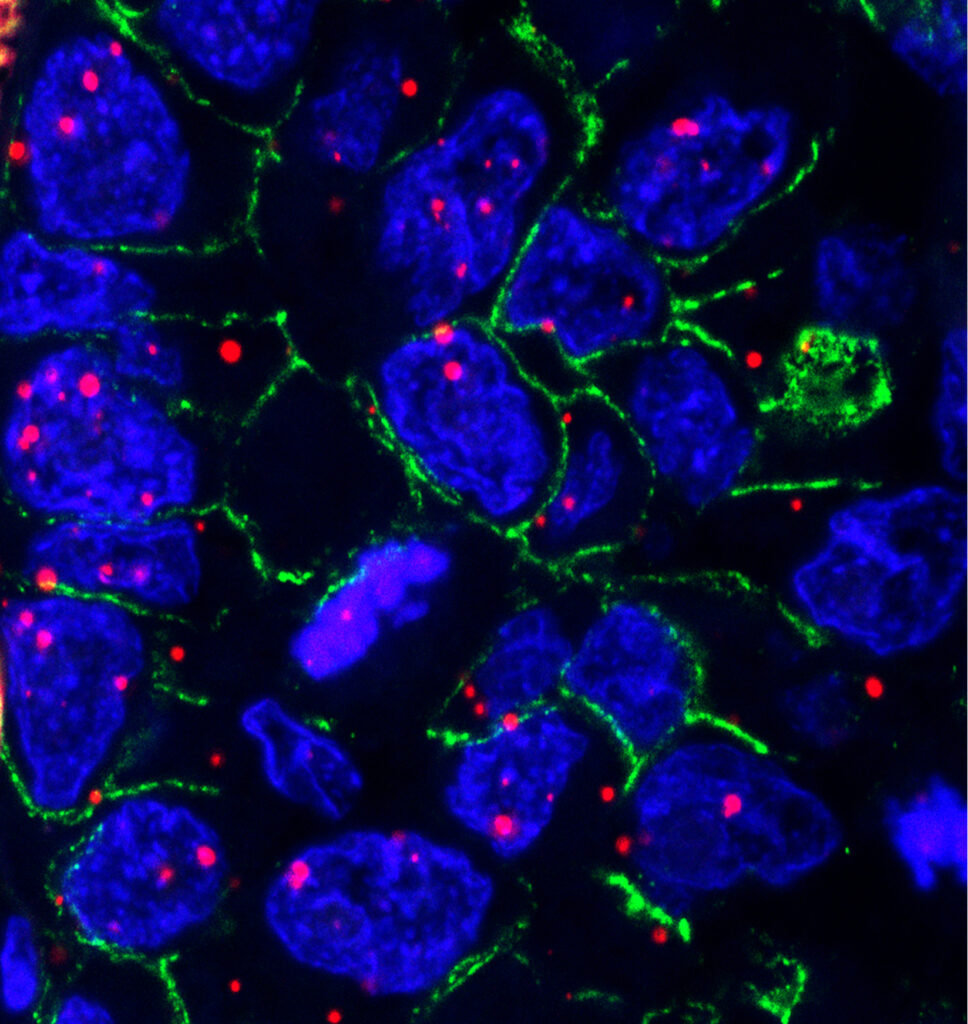
- A TME részletes karakterizálása immunhisztokémiával (IHC) és RNAscope assay-ekkel, valamint multiplexing technikákkal (Akoya’s Phenocycler, NanoString GeoMx Digital Spatial Profiler)
- Kifinomult scoring technikák kikészítése, számítógépes képanalízis és párhuzamos RNS-protein expressziós (spatial biology) adatfeldolgozás
- Fejlett többváltozós statisztikai modellek és machine learning algoritmusok alkalmazása a prognosztikus és prediktív biomarkerek azonosítához
Publikációink a témában:
Dora D, Megyesfalvi Z, Vörös I, Paál Á, Takacs P, Dobos D, Lőrincz B, Bokhari SMZ, Aloss K, Pallag G, Rivard C, Yu H, Hirsch FR, Görbe A, Varga ZV, Lohinai Z, Dome B. Expression of costimulatory molecule CD70 is prognostic in small cell lung cancer. Cancer Immunol Immunother. 2025 Apr 9;74(5):165.
Dora, David ; Vörös, Imre ; Varga, Zoltán V. ; Takacs, Peter ; Teglasi, Vanda ; Moldvay, Judit ; Lohinai, Zoltan ✉ BRAF RNA is prognostic and widely expressed in lung adenocarcinoma TRANSLATIONAL LUNG CANCER RESEARCH 12 : 1 pp. 27-41. , 15 p. (2023)
Dora, David ; Rivard, Christopher ; Yu, Hui ; Pickard, Shivaun Lueke ; Laszlo, Viktoria; Harko, Tunde ; Megyesfalvi, Zsolt ; Gerdan, Csongor ; Dinya, Elek ; Hoetzenecker, Konrad et al. Protein Expression of immune checkpoints STING and MHCII in small cell lung cancer. CANCER IMMUNOLOGY IMMUNOTHERAPY 72 : 3 pp. 561-578. , 18 p. (2023)
Lohinai, Zoltan ; Dora, David ✉ ; Caldwell, Charles ; Rivard, Christopher J. ; Suda, Kenichi ; Yu, Hui ; Rivalland, Gareth ; Ellison, Kim ; Rozeboom, Leslie ; Dziadziuszko, Rafal et al. Loss of STING expression is prognostic in non–small cell lung cancer JOURNAL OF SURGICAL ONCOLOGY 125 : 6 pp. 1042-1052. , 11 p. (2022)
Dora, David ; Rivard, Christopher ; Yu, Hui ; Picard, Shivaun Lueke ; Laszlo, Viktoria ; Harko, Tunde ; Megyesfalvi, Zsolt ; Dinya, Elek ; Gerdan, Csongor ; Szegvari, Gabor et al. Characterization of Tumor-associated Macrophages and the Immune Microenvironment in Limited-stage Neuroendocrine High-and -Low Small Cell Lung Cancer BIOLOGY-BASEL 10 : 6 Paper: 502 , 25 p. (2021)
David, Dora ; Rivard, Christopher ; Yu, Hui ; Bunn, Paul ; Suda, Kenichi ; Ren, Shengxiang ; Pickard, Shivaun Lueke ; Laszlo, Viktoria ; Harko, Tunde ; Megyesfalvi, Zsolt et al. Neuroendocrine subtypes of small cell lung cancer differ in terms of immune microenvironment and checkpoint molecule distribution MOLECULAR ONCOLOGY 14 : 9 pp. 1947-1965. , 19 p. (2020)
A bél mikrobiom hatása a tumorellenes immunitásra és az immunterápiára
A tüdőrák a rák okozta halálozások egyik vezető oka világszerte (az összes eset 11,6%-a), ahol az immunellenőrző pont gátló (ICI) monoterápiát vagy ICI kombinációkat gyakran alkalmazzák elsővonalbeli kezelésként az előrehaladott stádiumú és nem kissejtes tüdőrák (NSCLC) esetében. Jelenleg az 5 éves túlélési arány az NSCLC immunterápiával kezelt betegek körében egyetlen szerrel 30% a biomarkerrel kiválasztott (magas PD-L1 expressziójú) populációkban, és 10-20% a biomarkerrel nem kiválasztott csoportokban.
Az onkológia világába mára beférkőzött a mikrobiom kutatás is, ugyanis a bélmikrobiom egyre több kutatási eredmény alapján képes modulálni az immunrendszer rákellenes válaszait és a daganat mikrokörnyezetét. Erős bizonyítékok utalnak arra, hogy a bélben élő baktériumok közvetlenül befolyásolják a gasztrointesztinális tumorok kialakulását a diszbiózis révén, de tanulmányok más, nem bélrendszeri rákok esetében is kimutattak hasonló összefüggéseket, beleértve a tüdőrákot, amelyben a mi csoportunk is közölt korábban kutatási eredményeket. Továbbá az utóbbi időben intenzíven vizsgálják a bélmikrobiom szerepét a daganatellenes válaszok közvetítésében, különösen az immun- és kemoterápiás kezelések kapcsán. A kutatási projekt számos kulcs kérdésre keresi a választ: Melyek a tüdőrák immun mikrokörnyezetének specifikus jellemzői, és hogyan korrelálnak az immunterápia hatásosságával és a túléléssel? Hogyan korrelál a bél mikrobiomjának kompozíciója a tumor mikrokörnyezet tulajdonságaival és a kezelési eredményekkel? Milyen funkcionális állapotban vannak az immunsejtek a tumor mikrokörnyezetben, és van-e összefüggés köztük és mikrobiom között? A különböző lymphocyta-diszfunkciók összefüggésbe hozhatók-e egy specifikus taxonómiai vagy metabolikus bél- vagy intratumorális mikrobiommal? Képesek-e az új mikrobiális biomarkerek előre jelezni a beteg válaszát az immunterápiára?
A kutatás célja új prediktív és prognosztikus biomarkerek felfedezése a tumor mikrokörnyezetben és a bél mikrobiomban, amelyek elősegítik ezek interakcióinak megértését. Azáltal, hogy betekintést nyújtunk abba, hogyan befolyásolják a bél- és intratumorális mikróbák az anti-tumor immunitást és a daganatok progresszióját, ez a kutatás új távlatokat nyithat a mikrobiom-alapú rákterápiák számára.
A projekt központi céljai:
- A tumor mikrokörnyezet multiplex módszerekkel való karakterizálásából származó “spatial biology” adatok bélmikrobiommal való korrelációja
- Az intratumorális mikrobiom analízise és annak korrelációja a bélmikrobiommal, tumor mikrokörnyezettel és a betegek terápiás válaszával
- In vitro és egérkísérletek a statisztikailag kimutatott összefüggések validációjára
- Mikrobiális adjuváns immunterápiák kifejlesztése, azok preklinikai tesztelése tumoros egérmodelleken
Publikációink a témában:
Somodi C, Dora D, Horváth M, Szegvari G, Lohinai Z. Gut microbiome changes and cancer immunotherapy outcomes associated with dietary interventions: a systematic review of preclinical and clinical evidence. JOURNAL OF TRANSLATIONAL MEDICINE. 2025 Jul 8;23(1):756.
Dora D, Revisnyei P, Pasic A, Galffy G, Dulka E, Mihucz A, Roskó B, Szincsak S, Iliuk A, Weiss GJ, Lohinai Z. Host and bacterial urine proteomics might predict treatment outcomes for immunotherapy in advanced non-small cell lung cancer patients. FRONTIERS IN IMMUNOLOGY. 2025 Apr 14;16:1543817.
Dora, David., Kiraly, P., Somodi, C. Balazs, Ligeti; Edit, Dulka; Gabriella, Galffy; Zoltan, Lohinai ✉. Gut metatranscriptomics based de novo assembly reveals microbial signatures predicting immunotherapy outcomes in non-small cell lung cancer. JOURNAL OF TRANSLATIONAL MEDICINE 22, 1044 (2024).
Dora, David ✉ ; Szőcs, Emőke; Soós, Ádám; Halasy, Viktória; Somodi, Csenge; Mihucz, Anna; Rostás, Melinda; Mógor, Fruzsina; Lohinai, Zoltan; Nagy, Nándor From bench to bedside: an interdisciplinary journey through the gut-lung axis with insights into lung cancer and immunotherapy FRONTIERS IN IMMUNOLOGY 15 Paper: 1434804 , 29 p. (2024)
David, Dora ; Balazs, Ligeti ; Tamas, Kovacs ; Peter, Revisnyei ; Gabriella, Galffy ; Edit, Dulka ; Dániel, Krizsán ; Regina, Kalcsevszki ; Zsolt, Megyesfalvi ; Balazs, Dome ✉ ; Zoltan, Lohinai ✉. Non-Small Cell Lung Cancer Patients Treated with Anti-PD1 Immunotherapy Show Distinct Microbial Signatures and Metabolic Pathways According to Progression-free Survival and PD-L1 status ONCOIMMUNOLOGY 12 : 1 Paper: 2204746 , 15 p. (2023)
Dora, David; Weiss, Glen J; Megyesfalvi, Zsolt; Gállfy, Gabriella; Dulka, Edit; Kerpel-Fronius, Anna; Berta, Judit; Moldvay, Judit; Dome, Balazs ✉ ; Lohinai, Zoltan ✉ Computed Tomography-Based Quantitative Texture Analysis and Gut Microbial Community Signatures Predict Survival in Non-Small Cell Lung Cancer. CANCERS 15 : 20 Paper: 5091 , 19 p. (2023)
Dóra, Dávid ✉; Bokhari, Syeda Mahak Zahra; Aloss, Kenan; Takács, Péter; Desnoix, Juliane Zsuzsanna; Szklenárik, György; Hurley, Patrick Deniz; Lohinai, Zoltán ✉ Implication of the Gut Microbiome and Microbial-Derived Metabolites in Immune-Related Adverse Events: Emergence of Novel Biomarkers for Cancer Immunotherapy INTERNATIONAL JOURNAL OF MOLECULAR SCIENCES 24 : 3 Paper: 2769 , 26 p. (2023)
Könyvfejezet:
Dóra, D. A bélidegrendszer: bél-agy tengely In: Tulassay, Zsolt (szerk.) Gasztroenterológia Budapest, Magyarország : Medicina Könyvkiadó (2023) 1,180 p. pp. 14-23. , 10 p.
Eszközök, módszerek
- Immunhisztokémia (IHC), Immuncitokémia (ICC), Immunfluoreszcencia (IF) fagyasztott és formalin-fixált paraffinba ágyazott (FFPE) metszeteken
- RNAscope, RNAscope – IF multiplexing fagyasztott és FFPE metszeteken
- Rutin szövettani előkészítés, tissue-microarray (TMA)-k tervezése és készítésükben való részvétel
- Fejlett mikroszkópos scoring rendszerek fejlesztése, használata. Számítógépes képanalízis, morfometria kromogénnel és fluoreszcensen festett metszeteken. Konfokális mikroszkópia és képanalízis
- Multimodális spatial biology adatok elemzése QuPath és ImageJ szoftvercsomagokkal.
- Mikrobiom szekvenálási adat elemzés (Metagenome, metatranszkriptome). Nyers abundancia mátrixok előállítása, normalizálás, taxonómiai és diverzitás analízis. Metabolikus és transzkriptomikai pathway analízis MetaPhlan, Humann, Kraken és de novo assembly pipeline-ok használatával. Adatvizualizáció és magas szintű statisztikai modellek építése. Machine learning.
- Klinikai betegadat kezelés, adatbázis építés, adat menedzsment
- Egérkísérletek, azok előkészítése és egér szervek, szövetek eltávolítása, feldolgozása hisztológiai és downstream molekuláris analízis céljából