Új gyulladásos mechanizmusok akut iszkémia/reperfúziós károsodás és krónikus szívelégtelenség kialakulásában
Témacsoport vezető: Dr Varga Zoltán tudományos főmunkatárs (Google Scholar), Dr. Onódi Zsófia PhD hallgató, Dr. Vörös Imre PhD hallgató
A szívinfarktus következtében kialakuló krónikus szívelégtelenség prognózisa a modern terápiás eszközök és gyógyszerek mellett is igen rossz, a betegek mintegy fele a diagnózist követő 5 éven belül meghal. A betegség kezelése igen nagy terhet ró az egészségügyi rendszerekre.
A szívelégtelenség számos okból jöhet létre, de kialakulása során a szívizomzat struktúrája és funkcionalitása károsodik. Az eltérő etiológia ellenére a szívelégtelenség progressziójaban fontos szerepet játszanak mind celluláris (neutrophil granulociták, makrofágok, B és T limfociták) mind pedig humorális gyulladásos folyamatok, gyulladáskeltő citokinek, neuropeptidek, így az IL-1β, IL-18 vagy a TNF-α, melyek jelentősen fokozzák a szívizomzat károsodását. Vizsgálataink célja ezen sejttípusok és a különböző humorális faktorok terápiás modulálásának vizsgálata mind akut szívinfarktus modellekben, mind pedig az infarktust követő patológiás szívelégtelenségben.
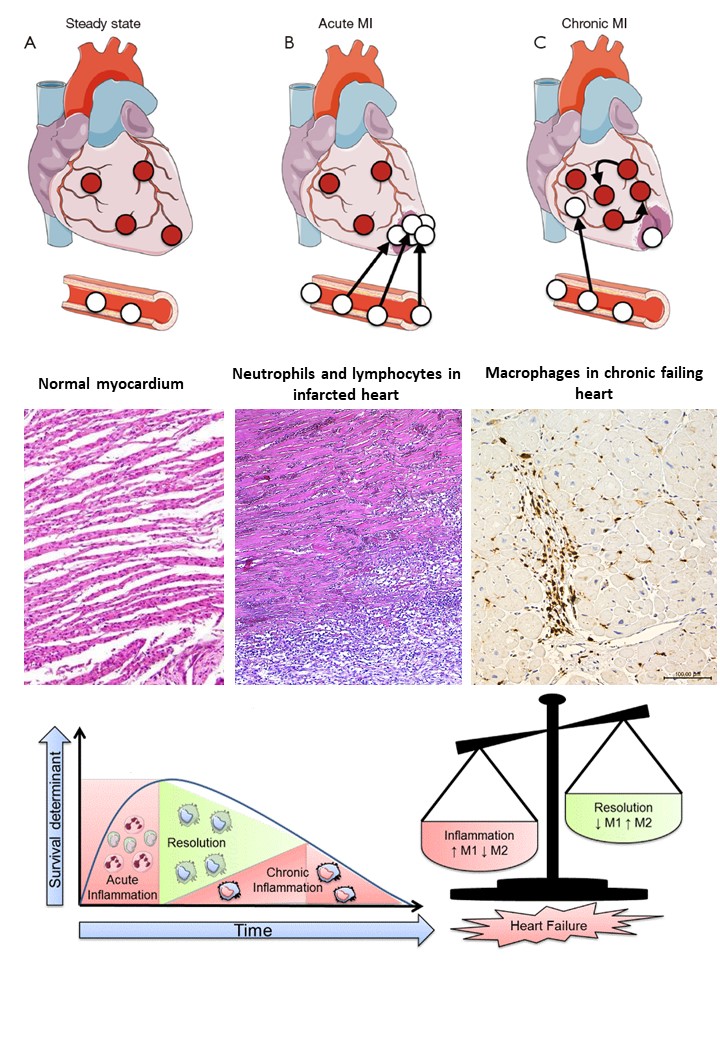 1. ábra: Szívinfarktust követően a károsodott szívizomzatot gyulladásos sejtek árasztják el, melyek hozzájárulhatnak a szív károsodásához (neutrofilek részt vesznek a fokozott szabadgyök képzésben) valamint bal karma krónikus remodellációjához is (makrofágok kiemelt szerepe a fibrotikus átalakulásban). A szövettani ábra bal oldalán normál szívizomzat látható, mellette középen nagy kiterjedésű infarktusos szívizomterület látható, ,melyet az infakrtust követően elözönlenek a neutrophil granulociták. Míg a jobb oldalon krónikus szívelégtelenségben szenvedő betegek szívéből készült metszeten a makrofágok megjelenése tapasztalható
1. ábra: Szívinfarktust követően a károsodott szívizomzatot gyulladásos sejtek árasztják el, melyek hozzájárulhatnak a szív károsodásához (neutrofilek részt vesznek a fokozott szabadgyök képzésben) valamint bal karma krónikus remodellációjához is (makrofágok kiemelt szerepe a fibrotikus átalakulásban). A szövettani ábra bal oldalán normál szívizomzat látható, mellette középen nagy kiterjedésű infarktusos szívizomterület látható, ,melyet az infakrtust követően elözönlenek a neutrophil granulociták. Míg a jobb oldalon krónikus szívelégtelenségben szenvedő betegek szívéből készült metszeten a makrofágok megjelenése tapasztalható
Elsajátítható képességek: hisztológiai technikák, immunohisztokémia, sejttenyésztés, fluoreszcens mikroszkóp kezelése, RNS és fehérje munkák – Western blot, qRT-PCR
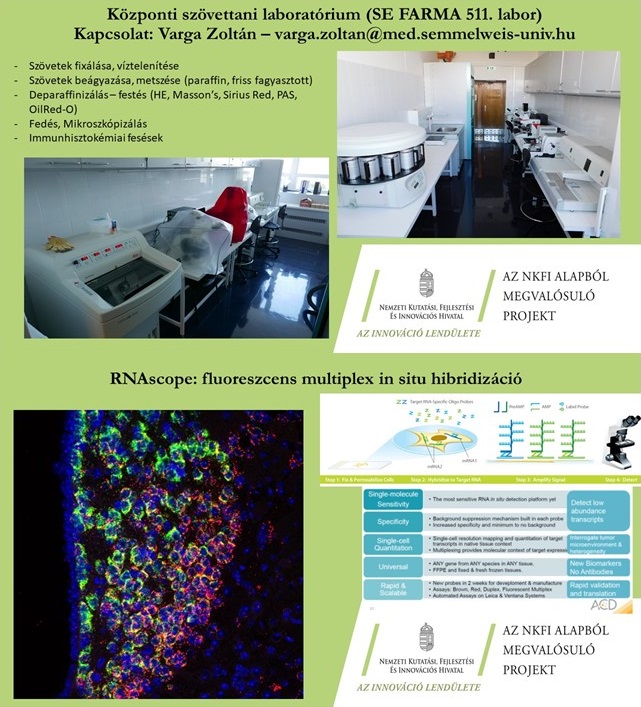 2. ábra: Hisztológiai laborunk
2. ábra: Hisztológiai laborunk
A témában megjelent közleményeink:
Humán szívelégtelen mintákon több fontos jelátviteli út szerepát vizsgáltuk, melyből már számos publikációnk jelent meg.
- Varga ZV, Pipicz M, Baán JA, Baranyai T, Koncsos G, Leszek P, Kuśmierczyk M, Sánchez-Cabo F, García-Pavía P, Brenner GJ, Giricz Z, Csont T, Mendler L, Lara-Pezzi E, Pacher P, Ferdinandy P. Alternative Splicing of NOX4 in the Failing Human Heart. Front Physiol. 2017 8:935. [IF: 3.394]
- Rajtik T, Goncalvesova E, Varga ZV, Leszek P, Kusmierczyk M, Hulman M, Kyselovic J, Ferdinandy P, Adameova A. Posttranslational modifications of calcium/calmodulin-dependent protein kinase IIδ and its downstream signaling in human failing hearts. Am J Transl Res. 20179:3573-3585. [IF: 3.061]
- Szobi A, Gonçalvesová E, Varga ZV, Leszek P, Kuśmierczyk M, Hulman M, Kyselovič J, Ferdinandy P, Adameová A. Analysis of necroptotic proteins in failing human hearts. J Transl Med. 2017 15:86. [IF: 4.197]
- Baán JA, Varga ZV, Leszek P, Kuśmierczyk M, Baranyai T, Dux L, Ferdinandy P, Braun T, Mendler L. Myostatin and IGF-I signaling in end-stage human heart failure: a qRT-PCR study. J Transl Med. 2015 16;13:1. [IF: 4.197]
Gyulladásos folyamatok vizsgálata metabolikus betegségekhez (elhízás, cukorbetegség, hiperkoleszterinémia, májcirrhózis) társuló szívizom diszfunkció kialakulásában
Témacsoport vezető: Dr Varga Zoltán tudományos főmunkatárs (Google Scholar), Dr. Bubenyák-Tóth Viktória posztdoktor kutató, Dr. Vörös Imre PhD hallgató
A szívelégtelenség a vezető halálokok közé tartozik világszerte. Klinikailag két markánsan elkülönülő formában jelentkezhet a betegség: csökkent ejekciós frakcióval (HFrEF) vagy megtartott ejekciós frakcióval (HFpEF). A szívelégtelenségben szenvedő betegek közel felénél HFpEF jelentkezik, azaz az ejekciós frakció megtartott. Ezek a betegek általában idősek és gyakran több társbetegségben szenvednek (pl.: diabétesz, elhízás, hiperkoleszterinémia). Sok esetben a betegek nem reagálnak jól a HFrEF kezelése során használt gyógyszerekre (digitálisz, ACE gátló, β blokkoló), emiatt igen jelentős az ezen a területen történő gyógyszerfejlesztés. A HFpEF-et jellemzi ezen felül a magas mortalitás (65% -os 5 éves mortalitás). Ezek az adatok alátámasztják, hogy kiemelten fontos a HFpEF mecahnizmusának jobb megértése a betegség kimenetelének javítása céljából.
HFpEF kialakulásának molekuláris mechanizmusa kevéssé ismert. Feltételezhető, hogy a kardiális diszfunkcióhoz hozzájárulhat egy szisztémás gyulladásos állapot, azonban ennek oki szerepe még nem bizonyított. Jelenlegi ismereteinket tovább korlátozza ezen komplex betegség állatkísérletes modellezésének nehézsége. Célunk ,ezért olyan új állatmodellek kifejlesztése és vizsgálata, melyek a HFpEF transzlációs vizsgálatát lehetővé teszik.
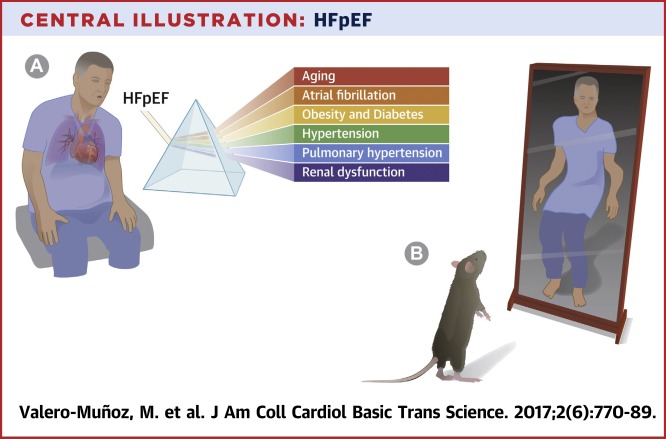 3. ábra: A HFpEF klinikai jellemzői
3. ábra: A HFpEF klinikai jellemzői
Elsajátítható képességek: munka kísérleti állatokkal, hisztológiai technikák, immunohisztokémia, RNS és fehérje munkák – Western blot, qRT-PCR
A témában megjelent közleményeink:
Elsőként alkalmaztunk droplet digital PCR és RNAScope in situ hybridizációs technikát perifáriás szövetekben (szívizom) G-protein kapcsolt receptorok expressziójának vizsgálatára. Ugyanebben a vizsgálatban elsőként tudtuk kimutatni egy érzékeny PET-ligand segítségével a CB1 receptor szintnövekedését kórósan elhízott betegek szívizomzatában
- Valenta I*, Varga ZV*, Valentine H, Cinar R, Horti A, Mathews WB, Dannals RF, Steele K, Kunos G, Wahl RL, Pomper MG, Wong DF, Pacher P, Schindler TH. Feasibility Evaluation of Myocardial Cannabinoid Type 1 Receptor Imaging in Obesity: A Translational Approach. JACC Cardiovasc Imaging. 2018 Feb;11(2 Pt 2):320-332. [IF: 10.189] *-megosztott elsőszerzőség
Elsőként írtuk le a miR-25 nevű mikorRNS szintjének csökkenését hiperkoleszterinémia hatására patkány szívizomzatban. A NOX4 nevű, szabadgyököket termelő enzimet azonosítottuk, mint a miR-25 fő targetjét. A miR25 szívizom diszfunckióban betöltött szerepét később két függetelen csoport is igazolta (egy Nature és egy Nature Cell Biology publikációban). Közlményünket az Elsevier kiadó ’Highly Cited’ kategóriába sorolta, az összesen kapott 91 citációja miatt.
- Varga ZV, Kupai K, Szűcs G, Gáspár R, Pálóczi J, Faragó N, Zvara A, Puskás LG, Rázga Z, Tiszlavicz L, Bencsik P, Görbe A, Csonka C, Ferdinandy P, Csont T.: MicroRNA-25-dependent up-regulation of NADPH oxidase 4 (NOX4) mediates hypercholesterolemia-induced oxidative/nitrative stress and subsequent dysfunction in the heart. J Mol Cell Cardiol. 2013. 62:111-21. [IF: 5.218]